Бендамустин выпадают ли волосы
Опубликовано: 17.09.2024
Содержание
- Структурная формула
- Английское название
- Латинское название вещества Бендамустин
- Фармакологическая группа вещества Бендамустин
- Нозологическая классификация (МКБ-10)
- Характеристика вещества Бендамустин
- Фармакология
- Применение вещества Бендамустин
- Противопоказания
- Ограничения к применению
- Побочные действия вещества Бендамустин
- Взаимодействие
- Пути введения
- Способ применения и дозы
- Взаимодействия с другими действующими веществами
- Торговые названия c действующим веществом Бендамустин
Структурная формула
Русское название
Английское название
Латинское название вещества Бендамустин
Химическое название
5-[бис-(2-хлорэтил)амино]-1'-метил-1Н-бензимидазол-2-бутановая кислота (в виде гидрохлорида)
Брутто-формула
Фармакологическая группа вещества Бендамустин
Нозологическая классификация (МКБ-10)
Код CAS
Характеристика вещества Бендамустин
Белый кристаллический порошок. Растворим в воде.
Фармакология
Механизм действия связан с переносом во время деления клетки алкильной группы в ДНК (положение 7-гуанина). Это приводит или к разрыву молекулы ДНК , или к связыванию двух цепей молекул. В результате нарушается жизнедеятельность клеток и процессы митоза. К препарату чувствительны клетки с гиперплазированными ядрами: опухолевые, лимфоидные и клетки костного мозга. После введения подвергается преобразованию в печени в активное алкилирующее соединение под воздействием оксидазной ферментной системы. В плазме крови с белками связывается незначительное количество. Т1/2 составляет 3–12 ч. Частично подвергается биотрансформации в печени с образованием неактивных метаболитов. Экскретируется почками как в неизмененном виде, так и в виде метаболитов.
Применение вещества Бендамустин
Генерализованная злокачественная лимфома, множественная миелома.
Противопоказания
Гиперчувствительность, гипопластическая анемия, опоясывающий лишай, генерализованные инфекции, нарушения функций печени, почек и сердечно-сосудистой системы, терминальная фаза заболевания, кахексия, беременность.
Ограничения к применению
Кормление грудью (на время лечения необходимо прекратить).
Побочные действия вещества Бендамустин
Аменорея, гипо- и азооспермия, лейкопения, суперинфекция, миоперикардит, геморрагический цистит, гиперурикемия, нефропатия, пневмофиброз, анемия, тромбоцитопения, геморрагический колит, холестатический гепатит, гипергликемия, алопеция, аллергические реакции; покраснение и болезненность в месте введения.
Взаимодействие
Усиливает влияние на костный мозг др. противоопухолевых средств, цитостатиков, иммуносупрессоров. Снижает эффективность противоподагрических препаратов.
Пути введения
Способ применения и дозы
В/в, вводится в виде 0,25% раствора по разработанным схемам.
Взаимодействия с другими действующими веществами
Торговые названия c действующим веществом Бендамустин
- Рибомустин
- РОЗУСТИН ®
Официальный сайт компании РЛС ® . Энциклопедия лекарств и товаров аптечного ассортимента российского интернета. Справочник лекарственных препаратов Rlsnet.ru предоставляет пользователям доступ к инструкциям, ценам и описаниям лекарственных средств, БАДов, медицинских изделий, медицинских приборов и других товаров. Фармакологический справочник включает информацию о составе и форме выпуска, фармакологическом действии, показаниях к применению, противопоказаниях, побочных действиях, взаимодействии лекарств, способе применения лекарственных препаратов, фармацевтических компаниях. Лекарственный справочник содержит цены на лекарства и товары фармацевтического рынка в Москве и других городах России.
Запрещена передача, копирование, распространение информации без разрешения правообладателя.
При цитировании информационных материалов, опубликованных на страницах сайта www.rlsnet.ru, ссылка на источник информации обязательна.
Еще много интересного
© РЕГИСТР ЛЕКАРСТВЕННЫХ СРЕДСТВ РОССИИ ® РЛС ® , 2000-2021.
Все права защищены.
Не разрешается коммерческое использование материалов.
Материалы сайта предназначены исключительно для медицинских и фармацевтических работников и носят справочно-информационный характер.
Фармакологическое действие
Бендамустин оказывает противоопухолевое, алкилирующее действие.
Фармакодинамика
Бендамустин является противоопухолевым препаратом с бифункциональной алкилирующей активностью. Механизм действия преимущественно связан с образованием перекрёстных сшивок молекул одноцепочечной и двухцепочечной ДНК вследствие алкилирования. В результате этого нарушается матричная функция ДНК и её синтез. Существуют также данные о том, что бендамустин обладает дополнительными антиметаболическими свойствами (эффектом пуринового аналога).
Антинеопластический эффект бендамустина был подтверждён в многочисленных исследованиях in vitro на различных опухолевых клеточных линиях (рак молочной железы, немелкоклеточный и мелкоклеточный рак лёгкого, рак яичников и различные виды лейкоза, а также рак толстой кишки, меланома, почечноклеточная карцинома, злокачественные новообразования предстательной железы и головного мозга) и in vivo — на различных экспериментальных моделях опухолей (меланома, рак молочной железы, саркома, лимфома, лейкоз и мелкоклеточный рак лёгкого). Бендамустин не демонстрирует или демонстрирует лишь в незначительной степени перекрёстную резистентность в человеческих опухолевых клеточных линиях с различными механизмами устойчивости.
Это частично объясняется взаимодействием с ДНК, которое, по сравнению с другими алкилирующими средствами, длится дольше (например, была обнаружена только частичная перекрёстная резистентность с другими алкилирующими средствами, такими как циклофосфамид, кармустин или цисплатин). Кроме того, в клинических исследованиях было обнаружено, что не существует полной перекрёстной резистентности между бендамустином и антрациклинами или алкилатами.
Фармакокинетика
После однократной 30-минутной внутривенной инфузии бендамустина в дозе 120 мг/м 2 поверхности тела бета-фаза элиминации (AUC1/2β) составляет 28,3 минуты. Объём распределения при 30-минутной внутривенной инфузии составляет 19,3 л, при последующем систематическом введении и достижении равновесной концентрации объём распределения составляет от 15,8 до 20,5 л. В системном Кровотоке бендамустин активно связывается с белками плазмы (>95 %), главным образом, с альбумином.
Способность бендамустина к связыванию с белками плазмы крови не нарушается при низких концентрациях альбумина в плазме крови, у пациентов в возрасте старше 70 лет и при поздних стадиях опухолей.
Метаболизм
Бендамустина гидрохлорид метаболизируется преимущественно в печени. Основным путём выведения бендамустина гидрохлорида из организма является его гидролиз с образованием моногидрокси- и дигидроксибендамустина. В образовании гамма-гидроксибендамустина (М3) и N-десметилбендамустина (М4) в печени задействован изофермент CYP 1А2 цитохрома P450. in vitro бендамустин не ингибирует CYP 1А4, CYP 2С9/10, CYP 2D6, CYP 2Е1 и CYP 3A4.
Выведение
Среднее значение общего клиренса после 30-минутной внутривенной инфузии препарата 12 субъектам в дозе 120 мг/м 2 поверхности тела составило 639.4 мл/мин. Около 20 % введённой дозы препарата экскретировалось почками на протяжении 24 часов. Количество экскретируемого с почками неизменённого бендамустина и его метаболитов располагается в порядке убывания следующим образом: моногидроксибендамустин > бендамустин > дигидроксибендамустин > окислённый метаболит > N-десметилбендамустин. С желчью выводятся преимущественно полярные метаболиты.
Фармакокинетика у различных групп пациентов
При 30-70 % опухолевом поражении печени и незначительно сниженной функции печени (сывороточный билирубин 10 мл/мин, в том числе находящихся на диализе, не отличались существенно от таковых у пациентов с нормальной функцией почек в отношении Cmax, Tmax, AUC, AUC1/2β, объёма распределения и выведения.
Пациенты старше 84 лет не включались в исследование фармакокинетики бендамустина, у лиц старше 18 и младше 84 лет фармакокинетические параметры значимо не различались.
Не обнаружено различий в фармакокинетике в зависимости от расы.
Показания
- Хронический лимфоцитарный лейкоз (эффективность применения в терапии первой линии по сравнению с другими химиопрепаратами кроме хлорамбуцила не была установлена).
- Индолентные неходжкинские лимфомы в монотерапии у пациентов, у которых наблюдалось прогрессирование на фоне или в течение 6 месяцев после окончания терапии с включением ритуксимаба и в комбинированной терапии в качестве терапии 1-ой линии.
- Терапия первой линии множественной миеломы (II стадия с прогрессированием или III стадия по Дьюри-Сальмону) в комбинации с преднизолоном для пациентов старше 65 лет, которым не показана аутологичная трансплантация стволовых клеток и у которых имеются клинические проявления нейропатии на момент постановки диагноза, препятствующие использованию терапии с включением талидомида или бортезомиба.
Противопоказания
- Повышенная чувствительность к бендамустину;
- умеренная и выраженная печёночная недостаточность;
- желтуха;
- количество нейтрофилов менее 1 500/мкл и/или тромбоцитов менее 75 000/мкл;
- хирургические вмешательства менее чем за 30 дней до начала терапии;
- инфекции, особенно сопровождающиеся лейкоцитопенией;
- беременность;
- лактация (период грудного вскармливания);
- детский возраст (отсутствие данных по эффективности и безопасности).
С осторожностью
- Лёгкая печёночная недостаточность;
- нарушения функции почек.
Пациенты с наличием в анамнезе серьёзных кардиологических заболеваний (инфаркт миокарда, эпизоды ишемии, аритмия) нуждаются в тщательном мониторинге водно-электролитного баланса, в особенности калия, и контроле ЭКГ в процессе терапии.
Беременность и грудное вскармливание
Применение при беременности
Специальных исследований о возможности применения бендамустина при беременности не проведено.
В экспериментальных исследованиях на животных выявлены признаки тератогенности и мутагенности.
Бендамустин противопоказан к применению при беременности.
Применение в период грудного вскармливания
В настоящее время нет данных о способности бендамустина проникать в грудное молоко.
На время лечения следует прекратить грудное вскармливание.
Планирование беременности
Мужчинам и женщинам на фоне терапии и как минимум в течение 6 месяцев после его окончания следует использовать надёжные методы контрацепции.
Мужчины до начала терапии бендамустином должны быть предупреждены о потенциальном риске для их репродуктивных способностей.
Мужчинам рекомендуется прибегнуть к криоконсервации спермы до начала лечения в связи с риском необратимого бесплодия, обусловленным применением бендамустина.
Способ применения и дозы
При индивидуальном подборе дозы следует руководствоваться данными специальной литературы.
Хронический лимфоцитарный лейкоз
Бендамустин 100 мг/м 2 внутривенно в виде 30-минутной инфузии в 1-й и 2-й дни каждого 28-дневного цикла (до 6 циклов).
В случае развития гематологической токсичности 3–4-й степени или негематологической токсичности ≥2-й степени выраженности введение бендамустина должно быть отложено как минимум до восстановления показателей абсолютного количества нейтрофилов ≥1 000/мкл и количества тромбоцитов ≥75 000/мкл и/или снижения степени выраженности негематологической токсичности до 1-й степени и менее.
Модификация доз при гематологической токсичности: при развитии токсичности 3–4-й степени доза препарата при последующих циклах должна быть снижена до 50 мг/м 2 . В случае повторного возникновения гематологической токсичности 3–4-й степени доза препарата должна быть снижена до 25 мг/м 2 .
Модификация доз при негематологической токсичности: при клинически выраженных признаках 3–4-й степени токсичности дозу Бендамустина при последующих циклах следует снизить до 50 мг/м 2 .
Неходжкинская лимфома
Монотерапия: бендамустин 120 мг/м 2 в виде 60-минутной инфузии в 1-й и 2-й дни каждого 21-дневного цикла (до 8 циклов).
Модификация доз при гематологической токсичности: при развитии токсичности 4-й степени доза препарата при последующих циклах должна быть снижена до 90 мг/м 2 . В случае повторного возникновения гематологической токсичности 4-й степени доза препарата должна быть снижена до 60 мг/м 2 .
Модификация доз при негематологической токсичности: при развитии токсичности 3–4-й степени дозу бендамустина при последующих циклах следует снизить до 90 мг/м 2 . В случае повторного возникновения негематологической токсичности 3–4-й степени доза препарата должна быть снижена до 60 мг/м 2 .
Комбинированная терапия: бендамустин в дозе 60 мг/м 2 поверхности тела внутривенно в виде 30-минутной инфузии ежедневно с 1-й по 5-й дни, винкристин внутривенно в 1-й день, преднизолон 100 мг/м 2 внутривенно ежедневно с 1-й по 5-й дни каждого 21-дневного цикла.
Применение у пациентов с нарушением функции печени
На основании фармакокинетических данных нет необходимости в коррекции дозы при концентрации билирубина в сыворотке крови 10 мл/мин.
Рекомендации по приготовлению раствора для инфузий
Содержимое флакона 25 мг разводят в 10 мл воды для инъекций и встряхивают до полного растворения.
Содержимое флакона 100 мг разводят в 40 мл воды для инъекций и встряхивают до полного растворения.
Полученный бесцветный прозрачный концентрат содержит 2,5 мг/мл бендамустина. После 5–10-минутной экспозиции необходимая доза бендамустина растворяется в 500 мл 0,9 % раствора натрия хлорида для инфузии. Химическая и физическая стабильность данного раствора сохраняется на протяжении 5 часов при комнатной температуре и 5 дней при хранении в холодильнике.
С микробиологической точки зрения препарат следует вводить сразу же после приготовления раствора, если метод разведения не исключает возможности его микробного обсеменения. Если готовый к использованию препарат не вводится сразу же после приготовления, ответственность за время и условия хранения готового раствора несёт приготовившее его лицо.
Побочные действия
Со стороны системы кроветворения
Очень часто — лейкопения, нейтропения, лимфоцитопения, анемия, тромбоцитопения; часто — кровотечения; очень редко — гемолиз.
Со стороны пищеварительной системы
Очень часто — тошнота, рвота, анорексия, воспаление слизистых оболочек желудочно-кишечного тракта, боль в животе, диспепсия; часто — диарея, запор, гастроэзофагеальный рефлюкс, сухость во рту, повышение активности аланинаминотрансферазы, аспартатаминотрансферазы, щелочной фосфатазы, концентрации билирубина; очень редко — геморрагический эзофагит, желудочно-кишечное кровотечение.
Со стороны сердечно-сосудистой системы
Часто — аритмия, тахикардия, снижение артериального давления; нечасто — выпот в полости перикарда; редко — острая сосудистая недостаточность; очень редко — инфаркт миокарда, сердечно-лёгочная недостаточность, флебит.
Со стороны дыхательной системы
Часто — нарушение функции дыхания, кашель, одышка, свистящее дыхание, назофарингит; очень редко — фиброз лёгких, первичная атипичная пневмония.
Со стороны нервной системы
Очень часто — головная боль, головокружение, бессонница; часто — нарушения вкуса, тревожность, депрессия; редко — повышенная сонливость, афония; очень редко — парестезии, периферическая сенсорная невропатия, антихолинэргический синдром, атаксия, энцефалит.
Дерматологические реакции
Очень часто — алопеция; часто — кожная сыпь, кожный зуд, сухость кожи, повышенная ночная потливость, гипергидроз; очень редко — эритема, дерматит, зуд, макулопапулёзная сыпь.
Со стороны костно-мышечной системы
Очень часто — боль в спине; часто — артралгия, боль в конечностях, боль в костях.
Аллергические реакции
Часто — реакции гиперчувствительности (аллергический дерматит, крапивница); редко — анафилактические/анафилактоидные реакции; очень редко — анафилактический шок.
Со стороны половой системы
Часто — аменорея; очень редко — бесплодие.
Местные реакции
Часто — боль в месте инъекции, эритема; редко — некроз окружающих тканей.
Прочие
Очень часто — повышение температуры тела, озноб, усиление болей, слабость, повышенная усталость, снижение массы тела, дегидратация, присоединение вторичных инфекций, гиперурикемия; часто — периферические отёки, гипокалиемия; редко — сепсис; очень редко — синдром лизиса опухоли.
При анализе данных по безопасности в зависимости от пола или расы не было выявлено клинически значимых различий.
Передозировка
Симптомы
При применении максимальной однократной дозы 280 мг/м 2 у пациентов на 7–21 день наблюдались нарушения на ЭКГ, включая удлинение интервала Q–T, синусовая тахикардия, изменения сегмента ST и зубца Т и блокада передней ветви левой ножки пучка Гиса.
Лечение
Специфический антидот неизвестен. В случае возможной передозировки следует тщательно наблюдать за пациентом, включая мониторинг гематологических показателей и показателей ЭКГ. Лечение симптоматическое. Диализ малоэффективен.
Взаимодействие
Бендамустин в комбинации с другими миелосупрессивными препаратами усиливает эффект подавления костного мозга и токсические свойства. Как и другие цитостатики, бендамустин подавляет выработку антител, усиливая риск инфекции при вакцинации.
Активные метаболиты бендамустина, гамма-гидроксибендамустин (М3) и N-десметил-бендамустин (М4) образуются под действием CYP1A2. Ингибиторы CYP1A2 (например, флувоксамин, ципрофлоксацин) потенциально могут увеличить концентрацию бендамустина и уменьшить концентрацию активных метаболитов в плазме крови. Индукторы CYP1A2 (например, омепразол, курение) потенциально могут уменьшить плазменные концентрации бендамустина и увеличить концентрацию его активных метаболитов в плазме крови. Следует соблюдать осторожность при одновременном применении ингибиторов или индукторов CYP1A2 или рассмотреть возможность альтернативного лечения.
Особые указания
Снижение лейкоцитов, нейтрофилов и тромбоцитов, как правило наблюдается на 14–20 день, восстановление — через 3–5 недель.
При использовании бендамустина отмечено изменение функции почек, поэтому во время лечения необходимо обеспечить тщательный мониторинг функции почек.
Лечение бендамустином следует проводить под наблюдением врача, имеющего опыт работы с противоопухолевыми препаратами.
На фоне терапии следует регулярно, как минимум один раз в неделю контролировать показатели периферической крови и показатели активности печёночных ферментов.
Бендамустин обладает тератогенным и мутагенным действием. Мужчинам и женщинам на фоне терапии и как минимум в течение 6 месяцев после его окончания следует использовать надёжные методы контрацепции. Мужчины до начала терапии бендамустином должны быть предупреждены о потенциальном риске для их репродуктивных способностей. Мужчинам рекомендуется прибегнуть к криоконсервации спермы до начала лечения в связи с риском необратимого бесплодия, обусловленным применением бендамустина.
При попадании на кожу и слизистые оболочки необходимо промыть их водой с мылом.
Влияние на способность к вождению автотранспорта и управлению механизмами
Исследования воздействия препарата на способность управлять транспортными средствами и механизмами не проводились. Однако во время терапии препаратом отмечались атаксия, периферическая невропатия, сонливость. Если подобные явления отмечаются, пациентам следует избегать управления транспортными средствами и работы с механизмами.
Полный текст:
- Аннотация
- Об авторах
- Список литературы
- Cited By
Аннотация
Введение. Бендамустин – один из основных препаратов, входящих в арсенал цитостатических агентов, которые используются в онкогематологии. В России препарат был зарегистрирован в конце 2010 г. под коммерческим названием Рибомустин (компании Astellas). В конце 2018 г. на российском рынке появились 2 отечественных дженерика бендамустина – Розустин® (Рафарма) и Ковада (Биокад).
Материалы и методы. В 2019 г. в отделение химиотерапии гемобластозов НМИЦ онкологии им. Н. Н. Блохина поступил препарат Розустин® (Рафарма, Россия). В данной работе представлен первый опыт применения Розустина® у пациентов с различными лимфопролиферативными заболеваниями. Чаще всего препарат использовался при рецидивах или рефрактерном течении классической лимфомы Ходжкина.
Результаты и заключение. Высокая непосредственная эффективность, приемлемый профиль токсичности по сравнению с альтернативными режимами «спасения», простота выполнения, возможность полноценного сбора гемопоэтических стволовых клеток с последующим проведением высокодозной химиотерапии с аутологичной трансплантацией гемопоэтических стволовых клеток подтверждают хороший потенциал комбинированной программы с включением препарата бендамустин (Розустин®).
Ключевые слова
Об авторах
Анастасия Александровна Семенова
Россия, 115478 Москва, Каширское шоссе, 24
Список литературы
1. Внутренние регламенты FDA на семь лет задержали выход дженериков бендамустина на рынок США. Fierma Pharma, 27 февраля 2019; Vademecum.
2. Rummel M.J., Niederle N., Maschmeyer G. et al. Bendamustine plus rituximab versus chop plus rituximab as first-line treatment for patients with indolent and mantle-cell lymphomas: an open-label, multicentre, randomized, phase 3 non-inferiority trial. Lancet 2013;381(9873):1203–10. DOI: 10.1016/S0140-6736(12)61763-2.
3. Visco C., Finotto S., Zambello R. et al. Combination of rituximab, bendamustine, and cytarabine for patients with mantlecell non-Hodgkin lymphoma ineligible for intensive regimens or autologous transplantation. J Clin Oncol 2013;31(11):1442–9. DOI: 10.1200/JCO.2012.45.9842.
4. Visco C., Chiappella A., Nassi L. et al. Rituximab, bendamustine, and low-dose cytarabine as induction therapy in elderly patients with mantle cell lymphoma: a multicentre, phase 2 trial from Fondazione Italiana Linfomi. Lancet Haematol 2017;4(1):e15–23. DOI: 10.1016/S2352-3026(16)30185-5.
5. Santoro A., Mazza R., Pulsoni A. et al. Bendamustine in combination with gemcitabine and vinorelbine is an effective regimen as induction chemotherapy before autologous stem-cell transplantation for relapsed or refractory Hodgkin lymphoma: final results of a multicenter phase II study. J Clin Oncol 2016;34(27):3293–9. DOI: 10.1200/jco.2016.66.4466.
6. Santoro A., Mazza R., Pulsoni A. et al. Five-year results of the BEGEV salvage regimen in relapsed/refractory classical Hodgkin lymphoma. Blood Adv 2020;4(1):136–40. DOI: 10.1182/bloodadvances.2019000984.
7. Ludwig H., Kasparu H., Leitgeb C. et al. Bendamustine-bortezomib-dexamethasone is an active and well-tolerated regimen in patients with relapsed or refractory multiple myeloma. Blood 2014;123(7):985–91. DOI: 10.1182/blood-2013-08-521468.
8. Berdeja J.G., Bauer T., Arrowsmith E. et al. Phase II study of bendamustine, bortezomib and dexamethasone (BBD) in the first-line treatment of patients with multiple myeloma who are not candidates for high dose chemotherapy. Br J Haematol 2017;177(2):254–62. DOI: 10.1111/bjh.14536.
9. Broccoli A., Argnani L., Botto B. et al. First salvage treatment with bendamustine and brentuximab vedotin in Hodgkin lymphoma: a phase 2 study of the Fondazione Italiana Linfomi. Blood Cancer J 2019;9(12):100. DOI: 10.1038/s41408-019-0265-x.
10. Baetz T., Belch A., Couban S. et al. Gemcitabine, dexamethasone and cisplatin is an active and non-toxic chemotherapy regimen in relapsed or refractory Hodgkin’s disease: a phase II study by the National cancer institute of Canada clinical trials group. Ann Oncol 2003;14(12):1762–7. DOI: 10.1093/annonc/mdg496.
11. Moskowitz C.H., Nimer S.D., Zelenetz A.D. et al. A 2-step comprehensive high-dose chemoradiotherapy second-line program for relapsed and refractory Hodgkin disease: analysis by intent to treat and development of a prognostic model. Blood 2001;97(3):616–23. DOI: 10.1182/blood.v97.3.616.
12. Josting A., Rudolph C., Reiser M. et al. Time-intensified dexamethasone/cisplatin/ cytarabine: an effective salvage therapy with low toxicity in patients with relapsed and refractory Hodgkin’s disease. Ann Oncol 2002;13(10):1628–35. DOI: 10.1093/annonc/mdf221.
13. Santoro A., Magagnoli M., Spina M. et al. Ifosfamide, gemcitabine, and vinorelbine: a new induction regimen for refractory and relapsed Hodgkin’s lymphoma. Haematologica 2007;92(1):35–41. DOI: 10.3324/haematol.10661.
14. Cheson B.D., Fisher R.I., Barrington S.F. et al. Recommendations for initial evaluation, staging, and response assessment of Hodgkin and non-Hodgkin’s lymphoma: the Lugano Classification. J Clin Oncol 2014;32(27):3059–67. DOI: 10.1200/jco.2013.54.8800.
15. Cheson B.D., Ansell S., Schwartz L. et al. Refinement of the Lugano Classification lymphoma response criteria in the era of immunomodulatory therapy. Blood 2016;128(21):2489–96. DOI: 10.1182/blood-2016-05-718528.
16. Corazzelli G., Angrilli F., D’Arco A. et al. Efficacy and safety of bendamustine for the treatment of patients with recurring Hodgkin lymphoma. Br J Haematol 2012; 160(2):207–15. DOI: 10.1111/bjh.12120.
17. Moskowitz A.J., Hamlin P.A.Jr, Perales M.A. et al. Phase II study of bendamustine in relapsed and refractory Hodgkin lymphoma. J Clin Oncol 2013;31(4):456–60. DOI: 10.1200/JCO.2012.45.3308.
18. Venkatesan P. Bendamustine combined regimen for Hodgkin’s lymphoma. Lancet Oncol 2016;17(8):e326. DOI: 10.1016/s1470-2045(16)30317-5.
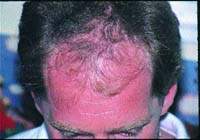
Какие факторы приводят к нарушению роста волос? Обратима ли алопеция, вызванная токсическим действием лекарственных препаратов? Возможно ли лечение медикаментозной алопеции? Воснове нарушения роста волос (их поредения различной степени выра
 |
Какие факторы приводят к нарушению роста волос?
Обратима ли алопеция, вызванная токсическим действием лекарственных препаратов?
Возможно ли лечение медикаментозной алопеции?
Воснове нарушения роста волос (их поредения различной степени выраженности), а также (реже) развития гипертрихоза лежат многочисленные эндогенные и экзогенные факторы. Среди последних немалую роль играет применение различных медикаментозных средств. При этом выпадение волос может наблюдаться не сразу, а через несколько недель или месяцев после начала приема лекарственного препарата или же начаться (либо стать) более выраженным после его отмены. Обычно при длительном применении того или иного препарата развивается диффузная алопеция, причем в патологический процесс вовлекается почти исключительно волосистая часть головы. Лишь в крайне редких случаях возможно развитие универсального облысения, что, в частности, наблюдается при приеме цитотоксических препаратов, например используемых при наличии у пациента опухолевого процесса.
Однако не во всех случаях выпадение волос определяется длительностью приема какого-либо лекарственного средства. Некоторые препараты, например непрямые антикоагулянты, дают такой эффект только в достаточно высоких дозах, а продолжительность терапии в развитии облысения не имеет существенного значения.
Механизм развития алопеции вследствие проведения какой-либо медикаментозной терапии в настоящее время до конца не ясен. Предполагается [5], что в его основе лежит взаимодействие активных субстанций лекарственных веществ с различными клетками, ответственными за рост волос, а именно фолликулярными кератиноцитами, клетками волосяного матрикса, а также соединительнотканными клетками, окружающими волосяную луковицу и перифолликулярные кровеносные сосуды. Наиболее часто мишенью для токсических эффектов лекарственных веществ становятся кератиноциты волосяных фолликулов. Это, как принято считать, обусловлено тем, что около 90% волосяных фолликулов находятся в фазе анагена, или фазе быстрого роста, а кроме того, интенсивный кровоток в кровеносных сосудах дермы, в частности в зоне волосяного сосочка, способствует повышению биодоступности и в ряде случаев токсичности активных ингредиентов [7, 14].
Помимо этого, кератиноциты волосяных фолликулов обладают выраженной способностью (значительно большей, чем кератиноциты эпидермиса) метаболизировать различные вещества, в первую очередь экзогенной природы [13]. Это обусловлено наличием в волосяных фолликулах различных ферментных систем, в частности цитохрома Р-450, локализованного в наружной мембране митохондрий, мембранах ядра и эндоплазматической сети и осуществляющего окисление неполярных органических соединений путем воздействия молекулярного кислорода. По мнению Boyd et al., 1983 [1], для того, чтобы проявился токсический эффект тех или иных веществ, последние должны взаимодействовать с различными клетками-мишенями после прохождения определенного метаболического пути.
Таким образом, кератиноциты волосяных фолликулов, обладая, с одной стороны, механизмами защиты от повреждающего действия экзогенных веществ и системой их элиминации, с другой стороны, в определенной степени способствуют проявлению токсического эффекта определенных лекарств. Вероятнее всего, что в большинстве случаев имеет место как непосредственное влияние активных субстанций лекарственных средств на митотически активные структуры волосяных фолликулов, замедление скорости кровотока в сосудах дермы и соответственно в волосяном сосочке, так и снижение концентрации в сыворотке крови и тканях липидов и белков и изменение их метаболических путей, а также микроэлементов, необходимых для нормального роста волос, вследствие образования хелатных комплексов, в первую очередь с ионами цинка и меди.
Однако одно и то же химическое соединение (лекарственное вещество) не во всех случаях вызывает развитие алопеции, и степень ее выраженности не всегда одинакова. Возможно, что это связано с особенностями взаимодействия между эндогенными и экзогенными факторами [11, 12].
Диффузная алопеция, обусловленная воздействием лекарственных препаратов, как правило, развивается не внезапно, а в течение нескольких месяцев после определенного латентного периода. В этот период отмечается постепенное уменьшение диаметра волосяной луковицы, замедление скорости роста волос. Развиваются дистрофические изменения волосяного стержня вследствие нарушения биосинтеза протеинов, характерным признаком которого является наличие у отрастающих волос заостренного кончика (по типу писчего пера). При анализе трихограммы у таких пациентов отмечается значительное повышение количества волос, фолликулы которых находятся в фазе телогена (30% и более). Однако провести дифференциальный диагноз между диффузной алопецией, индуцированной лекарственным воздействием на волосяной сосочек, и идиопатическим анагеновым или телогеновым выпадением волос очень трудно, так как данные трихограммы и гистологического исследования неспецифичны. В этих случаях правильной диагностике способствует анамнез. Кроме того, поставить верный диагноз может помочь возобновившееся выпадение волос при повторном назначении лекарственного средства, предположительно являющегося этиологическим фактором.
В большинстве случаев выпадение волос, вызванное применением того или иного лекарственного препарата, обратимо. Как правило, восстановление роста волос отмечается через несколько месяцев после прекращения воздействия этиологического фактора и зависит от степени выраженности изменений в волосяном фолликуле. Несмотря на то что обычно рост волос возобновляется самопроизвольно, по нашему мнению, целесообразно проводить соответствующую терапию, направленную на стимуляцию митотической активности клеток волосяной луковицы, синтез кератина и глобулярных протеинов межфибриллярного матрикса.
Лекарственные средства, прием которых может приводить к развитию облысения, широко используются в клинической практике дерматологов, кардиологов, гинекологов, терапевтов, психиатров и врачей других специальностей. Вообще, алопеция может возникнуть в результате применения любого лекарственного средства. Но было выявлено, что чаще всего усиленное выпадение волос наблюдается на фоне приема следующих групп препаратов [4, 6, 10]: витамин А и его производные; блокаторы бета-адренорецепторов (селективные и неселективные); блокаторы ангиотензин-конвертирующего фермента; антибактериальные препараты; нестероидные противовоспалительные средства; антикоагулянты; производные 6-аминохинолина; тиреостатические препараты; блокаторы гистаминовых Н2-рецепторов; нестероидные антиэстрогенные средства; препараты a-интерферона; производные имидазола; антидепрессанты; противосудорожные препараты; нейролептики; противопаркинсонические препараты; производные гидроксихлорохина; производные триазола; кетоконазол; урикостатические препараты; урикозурические препараты; пероральные контрацептивы; цитостатики; антигельминтные препараты; препараты лития; противогерпетические препараты; допаминомиметики (бромокриптин); депилятории (особенно в случае частого их использования на больных поверхностях); борная кислота.
При этом было отмечено, что из вышеуказанных препаратов значительно чаще диффузная алопеция развивается под влиянием противосудорожных препаратов, антидепрессантов, нейролептиков, витамина А и его синтетических производных, цитостатиков, b-блокаторов.
Так, цитостатические препараты, особенно при назначении их в больших дозах, приводят к практически полному прекращению митотического деления клеток волосяной луковицы.
Антибиотики, противогерпетические и другие средства могут нарушать связь матрикса и волосяного сосочка, что резко уменьшает продолжительность фазы анагена, и, следовательно, волосы значительно быстрее, чем в норме, переходят в фазу катагена, а затем в фазу телогена, что приводит к их интенсивному выпадению. В ряде случаев волосяные фолликулы не вступают в фазы катагена и телогена, а волосы выпадают в фазе анагена [2, 14]. Этот механизм, обусловливающий развитие состояния, называемого анагеновым выпадением волос, точно установлен для антикоагулянтов, препаратов, содержащих литий и борную кислоту. С помощью световой микроскопии по определенным признакам (длине корневой части волоса, наличию внутреннего и наружного корневых влагалищ, наличию или отсутствию пигмента в области волосяной колбы и др.) можно определить, на какой стадии произошло нарушение цикла развития волосяного фолликула.
Уменьшают продолжительность фазы роста (фазы анагена) пероральные контрацептивы [3]. Кроме повышения количества телогеновых волос в трихограмме, появления дистрофических волосяных фолликулов, возможно также изменение формы волосяного стержня (волнистые волосы становятся прямыми). В настоящее время причина этого не выяснена. Можно предположить, что так как форма волосяного стержня определяется наличием дисульфидных связей, образованных между прилежащими друг к другу серосодержащими аминокислотными остатками (в первую очередь цистеина и метионина) в полипептидах, входящих в структуру кератина, то изменение формы волоса происходит в результате полного или частичного разрушения этих связей. Это возможно, в частности, при изменении последовательности аминокислотных остатков, или, иными словами, первичной структуры кератина. Тот факт, что после отмены препаратов этой группы волосы не возвращаются к своему исходному состоянию в течение длительного периода времени (четырех и более лет), позволяет предположить развитие мутации в кератиновых генах. Кроме того, по данным клинических наблюдений, подобные нарушения формы волосяного стержня в основном отмечаются в лобно-теменной области, в то время как в затылочной области волосы сохраняют свой первоначальный вид. Как известно, при андрогенетической алопеции изменения волос (постепенное уменьшение размера волосянного фолликула и диаметра волосяного стержня с последующей заменой жесткого волоса на пушковый) наблюдаются также в лобно-теменной области, а затылочная остается интактной. Можно предположить, что в результате применения пероральных контрацептивов происходят изменения в рецепторном аппарате волосяного фолликула. Изменяется его чувствительность к действию гормонов, как и при андрогенетический алопеции, когда подобные изменения рецепторов детерминированы генетически.
Кроме того, пероральные контрацептивы способствуют снижению концентрации витамина В12 в сыворотке крови [8], что также ухудшает состояние волос.
В литературе имеются сообщения о том, что выпадение волос может вызвать применение никотиновой кислоты. С одной стороны, этот препарат обладает выраженным сосудорасширяющим эффектом, с другой, способствует снижению уровня холестерина в крови. Как известно, холестерин является одним из основных липидов, обнаруживаемых в дерме и, следовательно, в волосяном сосочке. Возможно, при этом происходят также изменения в процессе кератинизации, но до настоящего времени механизм действия никотиновой кислоты на рост волос не выяснен [9]. По нашим наблюдениям, никотиновая кислота и ее производные (ксантинола никотинат, теоникол), назначаемые короткими курсами (1–1,5 месяца) и в небольших дозах (0,15–0,3 г в сутки в зависимости от возраста) с целью стимуляции кровообращения в сосудах дермы при различной патологии волос, не вызывают их выпадения. По-видимому, этот эффект, как и при назначении витамина А, является дозозависимым.
Прием некоторых препаратов может вызвать избыточный рост волос, вначале пушковых, которые с течением времени трансформируются в жесткие. Этот эффект, который наиболее часто выражен в тех случаях, когда препарат назначается в значительных дозах и длительно, объясняется, вероятно, более быстрым переходом фазы телогена в фазу анагена. К ним относятся: кортикостероиды, миноксидил, циклоспорин А, D-пеницилламин, дифенилгидантоин, псорален.
Побочное действие этих препаратов давало возможность терапии некоторых форм алопеции, однако достигнутый эффект в подавляющем большинстве случаев оказывается нестойким, рецидив заболевания отмечается в среднем через три-четыре месяца после прекращения лечения. Кроме того, следует учитывать, что риск развития тяжелых побочных эффектов, которые наблюдаются практически у всех пациентов, в первую очередь у принимающих такие препараты, как системные кортикостероиды (а также местные при использовании их на больших поверхностях кожи) и циклоспорин А (в том числе и при локальном его применении), значительно превосходит положительное воздействие на течение алопеции.
Литература
1. Boyd M. R., Grygiel J. J., Miuchin R. F. Metabolic activation as a basis for organ selective toxicity // Clin. Exp. Pharmacol. Physiol. 10: 87-99, 1993.
2. Braun-Falco O. Klinik und Pathomechanismus der Endoxan-Alopecie als Bietrag zum Wesen cytostatischer Alopecien // Arch. Klin. Exp. Dermatol. 212:194-216, 1961.
3. Dawber R. P. R., Simpson N. B., Barth J. H. Oral contraceptives and the hair. Ch. 5, p. 130-131 in Dawber R. P. R. (ed). Diseases of the Hair and Scalp, 1997, 3d edition, Blackwell Science.
4. Dawber R. P. R. Diffuse Alopecia due to Chemicals and Endocrine Factors, Ch. 10.4, p. 411-417 in F. Camacho, W. Motagna Trichology, Disease of the Pilosebaceous Follicle, 1997, Biblioteca Aula Medica, Libros Princeps.
5. Ippen H. Haarausfall durch Medikamente // Dtsch. Med. Wochenschr. 95:1411-1416, 1970.
6. Merk H. F. Drugs Affecting Hair Growth, pp. 601-611 in Orfanos C. E., Happle R. (eds.) Hair and Hair Diseases. Springer-Verlag, 1990.
7. Orfanos C. E., Gerstein E. Haaransfall und Zytostatika // Arztl. Kosmet 6:96-105, 1976.
8. Ramsay I. D., Rushton D. H. Reduced serum vitamin B12 levels during oral cyproterone acetate and ethinyl oestradiol therapy in women with diffuse androgendependent alopecia // Clinical and Experimental Dermatology, 15, 277, 1990.
9. Reeves J. R. T., Maibach H. I. Drug and Chemical Induced Hair Loss. In: Mozzulli F. N., Mainbch H. I. (eds) Dermatotoxicology and Pharmacology. Halsred., New York, 1977.
10. Shelley W. B., Shelley E. D. Alopecia, 55-59 in Advanced Dermatological Therapy, W. B. Saunders Company, 1987.
11. Vesell E. S. Pharmacogenetics: multiple interactions between genes and environment as determinants of drug response // Am. J. Med. 66:183-187, 1983.
12. Vesell E. S., Penno M. B. Assesment of methods to identify sources of interindividual pharmacokinetic variations // Clin. Pharmacokinet. 3:378-409, 1983.
13. Wattenberg W., Leong J. C. Benzpyren hydroxylase in mouse skin //. Proc. Am. Assoc. Cancer Res., 11:81, 1970.
14. Zaum H., Neumann K., Werner G. Die Feistruktur dystrophischer Haare bei Vitamin A und Thallium Intoxikation. Hautarzt 23:544-550, 1972.
ИНСТРУКЦИЯ
по медицинскому применению лекарственного препарата
Торговое наименование препарата
Международное непатентованное наименование
Лекарственная форма
Порошок для приготовления концентрата для приготовления раствора для инфузий.
Состав
Описание
Лиофилизированный порошок белого цвета, микрокристаллический.
Фармакотерапевтическая группа
Противоопухолевый препарат, алкилирующее средство
Код АТХ
Фармакодинамика:
Бендамустин является противоопухолевым препаратом с бифункциональной алкилирующей активностью. Механизм действия преимущественно связан с образованием перекрестных сшивок молекул одноцепочечной и двухцепочечной ДНК вследствие алкилирования. В результате этого нарушается матричная функция ДНК и ее синтез. Существуют также данные о том что бендамустин обладает дополнительными антиметаболическими свойствами (эффектом пуринового аналога).
Антинеопластический эффект бендамустина был подтвержден в многочисленных исследованиях in vitro на различных опухолевых клеточных линиях (рак молочной железы немелкоклеточный и мелкоклеточный рак легкого рак яичников и различные виды лейкоза а также рак толстой кишки меланома почечноклеточная карцинома злокачественные новообразования предстательной железы и головного мозга) и in vivo - на различных экспериментальных моделях опухолей (меланома рак молочной железы саркома лимфома лейкоз и мелкоклеточный рак легкого). Бендамустин не демонстрирует или демонстрирует лишь в незначительной степени перекрестную резистентность в человеческих опухолевых клеточных линиях с различными механизмами устойчивости.
Это частично объясняется взаимодействием с ДНК которое по сравнению с другими алкилирующими средствами длится дольше (например была обнаружена только частичная перекрестная резистентность с другими алкилирующими средствами такими как циклофосфамид кармустин или цисплатин). Кроме того в клинических исследованиях было обнаружено что не существует полной перекрестной резистентности между бендамустином и антрациклинами или алкилатами.
Фармакокинетика:
После однократной 30-минутной внутривенной инфузии бендамустина в дозе 120 мг/м 2 поверхности тела бета-фаза элиминации (T1/2β) составляет 283 мин. Объем распределения при 30-минутной внутривенной инфузии составляет 193 л при последующем систематическом введении и достижении равновесной концентрации объем распределения
составляет от 158 до 205 л. В системном Кровотоке бендамустин активно связывается с белками плазмы (> 95%) главным образом с альбумином.
Способность бендамустина к связыванию с белками плазмы крови не нарушается при низких концентрациях альбумина в плазме крови у пациентов в возрасте старше 70 лет и при поздних стадиях опухолей.
Бендамустина гидрохлорид метаболизируется преимущественно в печени. Основным путем выведения бендамустина гидрохлорида из организма является его гидролиз с образованием моногидрокси- и дигидроксибендамустина. В образовании гамма-гидроксибендамустина (М3) и N-десметилбендамустина (М4) в печени задействован изофермент CYP 1А2 цитохрома Р450. In vitro бендамустин не ингибирует CYP 1А4 CYP 2С9/10 CYP 2D6 CYP 2Е1 и CYP ЗА4.
Элиминация и экскреция
Среднее значение общего клиренса после 30-минутной внутривенной инфузии препарата 12 субъектам в дозе 120 мг/м 2 поверхности тела составило 6394 мл/мин. Около 20 % введенной дозы препарата экскретировалось почками на протяжении 24 часов.
Количества экскретируемого с почками неизмененного бендамустина и его метаболитов располагается в порядке убывания следующим образом: моногидроксибендамустин > бендамустин > дигидроксибендамустин > окисленный метаболит > N-десметилбендамустин. С желчью выводятся преимущественно полярные метаболиты.
Фармакокинетика у различных групп пациентов
Пациенты с нарушенной функцией печени: при 30-70% опухолевом поражении печени и незначительно сниженной функцией печени (сывороточный билирубин Пациенты с нарушением функции почек: фармакокинетические параметры у пациентов с клиренсом креатинина >10 мл/мин в том числе находящиеся на диализе не отличались существенно от таковых у пациентов с нормальной функцией почек в отношении Сmах tmах АUСТ1/2β объема распределения и выведения.
Пожилые пациенты: пациенты старше 84 лет не включались в исследование фармакокинетики бендамустина у лиц старше 18 и младше 84 лет фармакокинетические параметры значимо не различались.
Не обнаружено различий в фармакокинетике в зависимости от расы.
Показания:
- Хронический лимфоцитарный лейкоз (эффективность применения в терапии первой линии по сравнению с другими химиопрепаратами кроме хлорамбуцила не была установлена).
- Индолентные неходжкинские лимфомы в монотерапии у пациентов у которых наблюдалось прогрессирование на фоне или в течение 6 месяцев после окончания терапии с включением ритуксимаба и в комбинированной терапии в качестве терапии 1-ой линии.
- Терапия первой линии множественной миеломы (II стадия с прогрессированием или III стадия по Дьюри-Сальмону) в комбинации с преднизолоном для пациентов старше 65 лет которым не показана аутологичная трансплантация стволовых клеток и у которых имеются клинические проявления нейропатии на момент постановки диагноза препятствующие использованию терапии с включением талидомида или бортезомиба.
Противопоказания:
- Гиперчувствительность к активному веществу или любому из вспомогательных компонентов или их непереносимость;
- Беременность и лактация;
- Умеренная и выраженная печеночная недостаточность;
- Количество нейтрофилов менее 1500/мкл и/или тромбоцитов менее 75000/мкл;
- Хирургические вмешательства менее чем за 30 дней до начала терапии;
- Инфекции особенно сопровождающиеся лейкоцитопенией;
- Детский возраст (отсутствие данных по эффективности и безопасности).
С осторожностью:
При легкой печеночной недостаточности при нарушениях функции почек.
Пациенты с наличием в анамнезе серьезных кардиологических заболеваний (инфаркт миокарда эпизоды ишемии аритмия) нуждаются в тщательном мониторинге водноэлектролитного баланса в особенности калия и контроле ЭКГ в процессе терапии Рибомустином.
Способ применения и дозы:
Побочные эффекты:
При анализе данных по безопасности в зависимости от пола или расы не было выявлено клинически значимых различий.
Нежелательные реакции перечислены по частоте их регистрации в соответствии со следующей градацией: часто: от > 1/100 до 1/1000 до 1/10 000 до 2 у пациентов на 7-21 день наблюдались нарушения на ЭКГ включая удлинение интервала Q-T синусовая тахикардия изменения сегмента ST и зубца Т и блокада передней ветви левой ножки пучка Гиса. Специфический антидот неизвестен. В случае возможной передозировки следует тщательно наблюдать за пациентом включая мониторинг гематологических показателей и показателей ЭКГ. Лечение симптоматическое. Диализ малоэффективен.
Взаимодействие:
Никаких специальных исследований лекарственных взаимодействий не проводилось. Активные метаболиты бендамустина гамма-гидроксибендамустин (М3) и N-десметил- бендамустин (М4) образуются под действием Р450 CYP1A2. Ингибиторы CYP1A2 (например флувоксамин ципрофлоксацин) потенциально могут увеличить концентрацию бендамустина и уменьшить концентрацию активных метаболитов в плазме крови. Индукторы CYP1A2 (например омепразол курение) потенциально могут уменьшить плазменные концентрации бендамустина и увеличить концентрацию его активных метаболитов в плазме крови. Следует соблюдать осторожность при одновременном применении ингибиторов или индукторов CYP1A2 или рассмотреть возможность альтернативного лечения.
Бендамустин в комбинации с другими миелосупрессивными препаратами усиливает эффект подавления костного мозга и токсические свойства. Как и другие цитостатики бендамустин подавляет выработку антител усиливая риск инфекции при вакцинации.
Особые указания:
Лечение Рибомустином следует проводить под наблюдением врача имеющего опыт работы с противоопухолевыми препаратами.
На фоне терапии следует регулярно как минимум один раз в неделю контролировать показатели периферической крови и показатели активности "печеночных" ферментов. Снижение лейкоцитов нейтрофилов и тромбоцитов как правило наблюдается на 14-20 день восстановление - через 3-5 недель.
При использовании Рибомустина отмечено изменение функции почек поэтому во время лечения необходимо обеспечить тщательный мониторинг функции почек.
В случае экстравазации инфузию следует немедленно прекратить с последующим охлаждением места введения и поднятием руки где произошла экстравазация. Оставшийся препарат должен быть введен в другую вену.
Бендамустин обладает тератогенным и мутагенным действием. Пациентам на фоне терапии и как минимум в течение 6-ти месяцев после его окончания следует использовать надежные методы контрацепции. Мужчинам рекомендуется прибегнуть к криоконсервации спермы до начала лечения в связи с риском бесплодия обусловленным применением данного препарата. При попадании на кожу и слизистые оболочки необходимо промыть их водой с мылом.
Влияние на способность управлять трансп. ср. и мех.:
Форма выпуска/дозировка:
Порошок для приготовления концентрата для приготовления раствора для инфузий 25 мг и 100 мг.
Упаковка:
Дозировка 25 мг: по 55 мг лиофилизированного порошка во флакон из коричневого стекла I типа объемом 26 мл с резиновой пробкой и развальцованным съемным алюминиевым колпачком предназначенным только для однократного использования. По 1 5 10 или 20 флаконов вместе с инструкцией по применению в картонную пачку.
Дозировка 100 мг: по 220 мг лиофилизированного порошка во флакон из коричневого стекла I типа объемом 60 мл с резиновой пробкой и развальцованным съемным алюминиевым колпачком предназначенным только для однократного использования. По 1 или 5 флаконов вместе с инструкцией по применению в картонную пачку.
Условия хранения:
В защищенном от света месте при температуре не выше 25 °С.
Хранить в недоступном для детей месте.
Срок годности:
Не использовать по истечении срока годности.
Условия отпуска
Производитель
Теммлер Верке ГмбХ, Weihenstephanerstrasse 28, 81637 Munchen, Germany, Германия
Читайте также:

