Могут ли от сиофора выпадать волосы
Опубликовано: 17.09.2024
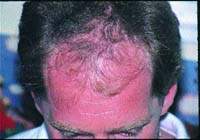
Какие факторы приводят к нарушению роста волос? Обратима ли алопеция, вызванная токсическим действием лекарственных препаратов? Возможно ли лечение медикаментозной алопеции? Воснове нарушения роста волос (их поредения различной степени выра
 |
Какие факторы приводят к нарушению роста волос?
Обратима ли алопеция, вызванная токсическим действием лекарственных препаратов?
Возможно ли лечение медикаментозной алопеции?
Воснове нарушения роста волос (их поредения различной степени выраженности), а также (реже) развития гипертрихоза лежат многочисленные эндогенные и экзогенные факторы. Среди последних немалую роль играет применение различных медикаментозных средств. При этом выпадение волос может наблюдаться не сразу, а через несколько недель или месяцев после начала приема лекарственного препарата или же начаться (либо стать) более выраженным после его отмены. Обычно при длительном применении того или иного препарата развивается диффузная алопеция, причем в патологический процесс вовлекается почти исключительно волосистая часть головы. Лишь в крайне редких случаях возможно развитие универсального облысения, что, в частности, наблюдается при приеме цитотоксических препаратов, например используемых при наличии у пациента опухолевого процесса.
Однако не во всех случаях выпадение волос определяется длительностью приема какого-либо лекарственного средства. Некоторые препараты, например непрямые антикоагулянты, дают такой эффект только в достаточно высоких дозах, а продолжительность терапии в развитии облысения не имеет существенного значения.
Механизм развития алопеции вследствие проведения какой-либо медикаментозной терапии в настоящее время до конца не ясен. Предполагается [5], что в его основе лежит взаимодействие активных субстанций лекарственных веществ с различными клетками, ответственными за рост волос, а именно фолликулярными кератиноцитами, клетками волосяного матрикса, а также соединительнотканными клетками, окружающими волосяную луковицу и перифолликулярные кровеносные сосуды. Наиболее часто мишенью для токсических эффектов лекарственных веществ становятся кератиноциты волосяных фолликулов. Это, как принято считать, обусловлено тем, что около 90% волосяных фолликулов находятся в фазе анагена, или фазе быстрого роста, а кроме того, интенсивный кровоток в кровеносных сосудах дермы, в частности в зоне волосяного сосочка, способствует повышению биодоступности и в ряде случаев токсичности активных ингредиентов [7, 14].
Помимо этого, кератиноциты волосяных фолликулов обладают выраженной способностью (значительно большей, чем кератиноциты эпидермиса) метаболизировать различные вещества, в первую очередь экзогенной природы [13]. Это обусловлено наличием в волосяных фолликулах различных ферментных систем, в частности цитохрома Р-450, локализованного в наружной мембране митохондрий, мембранах ядра и эндоплазматической сети и осуществляющего окисление неполярных органических соединений путем воздействия молекулярного кислорода. По мнению Boyd et al., 1983 [1], для того, чтобы проявился токсический эффект тех или иных веществ, последние должны взаимодействовать с различными клетками-мишенями после прохождения определенного метаболического пути.
Таким образом, кератиноциты волосяных фолликулов, обладая, с одной стороны, механизмами защиты от повреждающего действия экзогенных веществ и системой их элиминации, с другой стороны, в определенной степени способствуют проявлению токсического эффекта определенных лекарств. Вероятнее всего, что в большинстве случаев имеет место как непосредственное влияние активных субстанций лекарственных средств на митотически активные структуры волосяных фолликулов, замедление скорости кровотока в сосудах дермы и соответственно в волосяном сосочке, так и снижение концентрации в сыворотке крови и тканях липидов и белков и изменение их метаболических путей, а также микроэлементов, необходимых для нормального роста волос, вследствие образования хелатных комплексов, в первую очередь с ионами цинка и меди.
Однако одно и то же химическое соединение (лекарственное вещество) не во всех случаях вызывает развитие алопеции, и степень ее выраженности не всегда одинакова. Возможно, что это связано с особенностями взаимодействия между эндогенными и экзогенными факторами [11, 12].
Диффузная алопеция, обусловленная воздействием лекарственных препаратов, как правило, развивается не внезапно, а в течение нескольких месяцев после определенного латентного периода. В этот период отмечается постепенное уменьшение диаметра волосяной луковицы, замедление скорости роста волос. Развиваются дистрофические изменения волосяного стержня вследствие нарушения биосинтеза протеинов, характерным признаком которого является наличие у отрастающих волос заостренного кончика (по типу писчего пера). При анализе трихограммы у таких пациентов отмечается значительное повышение количества волос, фолликулы которых находятся в фазе телогена (30% и более). Однако провести дифференциальный диагноз между диффузной алопецией, индуцированной лекарственным воздействием на волосяной сосочек, и идиопатическим анагеновым или телогеновым выпадением волос очень трудно, так как данные трихограммы и гистологического исследования неспецифичны. В этих случаях правильной диагностике способствует анамнез. Кроме того, поставить верный диагноз может помочь возобновившееся выпадение волос при повторном назначении лекарственного средства, предположительно являющегося этиологическим фактором.
В большинстве случаев выпадение волос, вызванное применением того или иного лекарственного препарата, обратимо. Как правило, восстановление роста волос отмечается через несколько месяцев после прекращения воздействия этиологического фактора и зависит от степени выраженности изменений в волосяном фолликуле. Несмотря на то что обычно рост волос возобновляется самопроизвольно, по нашему мнению, целесообразно проводить соответствующую терапию, направленную на стимуляцию митотической активности клеток волосяной луковицы, синтез кератина и глобулярных протеинов межфибриллярного матрикса.
Лекарственные средства, прием которых может приводить к развитию облысения, широко используются в клинической практике дерматологов, кардиологов, гинекологов, терапевтов, психиатров и врачей других специальностей. Вообще, алопеция может возникнуть в результате применения любого лекарственного средства. Но было выявлено, что чаще всего усиленное выпадение волос наблюдается на фоне приема следующих групп препаратов [4, 6, 10]: витамин А и его производные; блокаторы бета-адренорецепторов (селективные и неселективные); блокаторы ангиотензин-конвертирующего фермента; антибактериальные препараты; нестероидные противовоспалительные средства; антикоагулянты; производные 6-аминохинолина; тиреостатические препараты; блокаторы гистаминовых Н2-рецепторов; нестероидные антиэстрогенные средства; препараты a-интерферона; производные имидазола; антидепрессанты; противосудорожные препараты; нейролептики; противопаркинсонические препараты; производные гидроксихлорохина; производные триазола; кетоконазол; урикостатические препараты; урикозурические препараты; пероральные контрацептивы; цитостатики; антигельминтные препараты; препараты лития; противогерпетические препараты; допаминомиметики (бромокриптин); депилятории (особенно в случае частого их использования на больных поверхностях); борная кислота.
При этом было отмечено, что из вышеуказанных препаратов значительно чаще диффузная алопеция развивается под влиянием противосудорожных препаратов, антидепрессантов, нейролептиков, витамина А и его синтетических производных, цитостатиков, b-блокаторов.
Так, цитостатические препараты, особенно при назначении их в больших дозах, приводят к практически полному прекращению митотического деления клеток волосяной луковицы.
Антибиотики, противогерпетические и другие средства могут нарушать связь матрикса и волосяного сосочка, что резко уменьшает продолжительность фазы анагена, и, следовательно, волосы значительно быстрее, чем в норме, переходят в фазу катагена, а затем в фазу телогена, что приводит к их интенсивному выпадению. В ряде случаев волосяные фолликулы не вступают в фазы катагена и телогена, а волосы выпадают в фазе анагена [2, 14]. Этот механизм, обусловливающий развитие состояния, называемого анагеновым выпадением волос, точно установлен для антикоагулянтов, препаратов, содержащих литий и борную кислоту. С помощью световой микроскопии по определенным признакам (длине корневой части волоса, наличию внутреннего и наружного корневых влагалищ, наличию или отсутствию пигмента в области волосяной колбы и др.) можно определить, на какой стадии произошло нарушение цикла развития волосяного фолликула.
Уменьшают продолжительность фазы роста (фазы анагена) пероральные контрацептивы [3]. Кроме повышения количества телогеновых волос в трихограмме, появления дистрофических волосяных фолликулов, возможно также изменение формы волосяного стержня (волнистые волосы становятся прямыми). В настоящее время причина этого не выяснена. Можно предположить, что так как форма волосяного стержня определяется наличием дисульфидных связей, образованных между прилежащими друг к другу серосодержащими аминокислотными остатками (в первую очередь цистеина и метионина) в полипептидах, входящих в структуру кератина, то изменение формы волоса происходит в результате полного или частичного разрушения этих связей. Это возможно, в частности, при изменении последовательности аминокислотных остатков, или, иными словами, первичной структуры кератина. Тот факт, что после отмены препаратов этой группы волосы не возвращаются к своему исходному состоянию в течение длительного периода времени (четырех и более лет), позволяет предположить развитие мутации в кератиновых генах. Кроме того, по данным клинических наблюдений, подобные нарушения формы волосяного стержня в основном отмечаются в лобно-теменной области, в то время как в затылочной области волосы сохраняют свой первоначальный вид. Как известно, при андрогенетической алопеции изменения волос (постепенное уменьшение размера волосянного фолликула и диаметра волосяного стержня с последующей заменой жесткого волоса на пушковый) наблюдаются также в лобно-теменной области, а затылочная остается интактной. Можно предположить, что в результате применения пероральных контрацептивов происходят изменения в рецепторном аппарате волосяного фолликула. Изменяется его чувствительность к действию гормонов, как и при андрогенетический алопеции, когда подобные изменения рецепторов детерминированы генетически.
Кроме того, пероральные контрацептивы способствуют снижению концентрации витамина В12 в сыворотке крови [8], что также ухудшает состояние волос.
В литературе имеются сообщения о том, что выпадение волос может вызвать применение никотиновой кислоты. С одной стороны, этот препарат обладает выраженным сосудорасширяющим эффектом, с другой, способствует снижению уровня холестерина в крови. Как известно, холестерин является одним из основных липидов, обнаруживаемых в дерме и, следовательно, в волосяном сосочке. Возможно, при этом происходят также изменения в процессе кератинизации, но до настоящего времени механизм действия никотиновой кислоты на рост волос не выяснен [9]. По нашим наблюдениям, никотиновая кислота и ее производные (ксантинола никотинат, теоникол), назначаемые короткими курсами (1–1,5 месяца) и в небольших дозах (0,15–0,3 г в сутки в зависимости от возраста) с целью стимуляции кровообращения в сосудах дермы при различной патологии волос, не вызывают их выпадения. По-видимому, этот эффект, как и при назначении витамина А, является дозозависимым.
Прием некоторых препаратов может вызвать избыточный рост волос, вначале пушковых, которые с течением времени трансформируются в жесткие. Этот эффект, который наиболее часто выражен в тех случаях, когда препарат назначается в значительных дозах и длительно, объясняется, вероятно, более быстрым переходом фазы телогена в фазу анагена. К ним относятся: кортикостероиды, миноксидил, циклоспорин А, D-пеницилламин, дифенилгидантоин, псорален.
Побочное действие этих препаратов давало возможность терапии некоторых форм алопеции, однако достигнутый эффект в подавляющем большинстве случаев оказывается нестойким, рецидив заболевания отмечается в среднем через три-четыре месяца после прекращения лечения. Кроме того, следует учитывать, что риск развития тяжелых побочных эффектов, которые наблюдаются практически у всех пациентов, в первую очередь у принимающих такие препараты, как системные кортикостероиды (а также местные при использовании их на больших поверхностях кожи) и циклоспорин А (в том числе и при локальном его применении), значительно превосходит положительное воздействие на течение алопеции.
Литература
1. Boyd M. R., Grygiel J. J., Miuchin R. F. Metabolic activation as a basis for organ selective toxicity // Clin. Exp. Pharmacol. Physiol. 10: 87-99, 1993.
2. Braun-Falco O. Klinik und Pathomechanismus der Endoxan-Alopecie als Bietrag zum Wesen cytostatischer Alopecien // Arch. Klin. Exp. Dermatol. 212:194-216, 1961.
3. Dawber R. P. R., Simpson N. B., Barth J. H. Oral contraceptives and the hair. Ch. 5, p. 130-131 in Dawber R. P. R. (ed). Diseases of the Hair and Scalp, 1997, 3d edition, Blackwell Science.
4. Dawber R. P. R. Diffuse Alopecia due to Chemicals and Endocrine Factors, Ch. 10.4, p. 411-417 in F. Camacho, W. Motagna Trichology, Disease of the Pilosebaceous Follicle, 1997, Biblioteca Aula Medica, Libros Princeps.
5. Ippen H. Haarausfall durch Medikamente // Dtsch. Med. Wochenschr. 95:1411-1416, 1970.
6. Merk H. F. Drugs Affecting Hair Growth, pp. 601-611 in Orfanos C. E., Happle R. (eds.) Hair and Hair Diseases. Springer-Verlag, 1990.
7. Orfanos C. E., Gerstein E. Haaransfall und Zytostatika // Arztl. Kosmet 6:96-105, 1976.
8. Ramsay I. D., Rushton D. H. Reduced serum vitamin B12 levels during oral cyproterone acetate and ethinyl oestradiol therapy in women with diffuse androgendependent alopecia // Clinical and Experimental Dermatology, 15, 277, 1990.
9. Reeves J. R. T., Maibach H. I. Drug and Chemical Induced Hair Loss. In: Mozzulli F. N., Mainbch H. I. (eds) Dermatotoxicology and Pharmacology. Halsred., New York, 1977.
10. Shelley W. B., Shelley E. D. Alopecia, 55-59 in Advanced Dermatological Therapy, W. B. Saunders Company, 1987.
11. Vesell E. S. Pharmacogenetics: multiple interactions between genes and environment as determinants of drug response // Am. J. Med. 66:183-187, 1983.
12. Vesell E. S., Penno M. B. Assesment of methods to identify sources of interindividual pharmacokinetic variations // Clin. Pharmacokinet. 3:378-409, 1983.
13. Wattenberg W., Leong J. C. Benzpyren hydroxylase in mouse skin //. Proc. Am. Assoc. Cancer Res., 11:81, 1970.
14. Zaum H., Neumann K., Werner G. Die Feistruktur dystrophischer Haare bei Vitamin A und Thallium Intoxikation. Hautarzt 23:544-550, 1972.

Метформин – это лекарство, используемое для лечения диабета 2 типа и его профилактики, если существует высокий риск развития болезни. Средство также используется при лечении синдрома поликистозных яичников, хотя во многих странах препарат для этих целей официально не одобрен.
Получая рецепт у эндокринолога, пациенты, часто интересуются, как работает метформин и какие у него побочные эффекты.
Метформин – действие при диабете 2 типа
Метформин – широко используемый препарат, который имеет явные преимущества с точки зрения влияния на метаболизм глюкозы и минимизации осложнений, связанных с диабетом. Механизм действия этого лекарства разнонаправлен, и если быть честными, до сих пор до конца не изучен. Но количество доказанных эффектов уже говорит о высокой ценности этого средства.
Ключевым органом-мишенью для этого препарата является печень. Улучшение гликемической ценности происходит благодаря влиянию действующего вещества на процесс глюконеогенеза, который состоит в превращении аминокислот и других соединений в глюкозу. С другой стороны, ингибируется поглощение сахара в тонкой кишке. Дополняет гипогликемическую активность увеличение периферического поглощения глюкозы.
Также доказан ряд других преимуществ использования этого гипогликемического препарата. Метформин уменьшает адгезию клеток крови к стенке кровеносных сосудов и секрецию эндотелиальных факторов активации, предотвращая развитие атеросклероза.
Уменьшение концентрации провоспалительных цитокинов и количества свободных кислородных радикалов вызывает противовоспалительный эффект.
Метформин известен своим благоприятным воздействием на продолжительность жизни и на нарушения, вызванные повышенной резистентностью к инсулину. По этой причине его классифицируют как препарат первой линии в группе эффективных препаратов для лечения диабета 2 типа.
Метформин – показания
Метформин имеет множество терапевтических применений. Согласно последним рекомендациям, он должен назначаться на каждом этапе лечения диабета 2 типа. Его можно использовать как отдельно, так и в сочетании с другими оральными гипогликемическими средствами или инсулином.
Метформин назначается в качестве препарата первой линии, особенно для пациентов с ожирением, кому в достижении адекватного контроля гликемии не помогло соблюдение диеты и физических упражнений.
Препарат также может быть назначен пациентам с диабетом в сочетании с диагностированным сердечно-сосудистым заболеванием или хроническим заболеванием почек. Метформин и его аналоги отлично сочетаются с другими лекарственными препаратами в тройном режиме комбинированной терапии без инсулина.
Вещество также используется при синдроме поликистозных яичников (СПКЯ), так как доказано, что в число причин этого заболевания является резистентность к инсулину с вторичной гиперинсулинемией. Кроме того, терапия снижает избыточный вес и ожирение, что очень часто встречается у женщин с СПКЯ.
Препарат метформин также включен в список фармакологических средств, способствующих снижению веса у людей с диабетическими расстройствами. Во многих исследованиях наблюдается снижение веса после первого года лечения на 2 кг. Но лекарство нельзя использовать как единственное средство для похудения.
Метформин – препараты и дозировка (страны Европы)
Метформин выпускается в таблетках, содержащих 500 мг, 850 мг и 1000 мг активного вещества. Все лекарства отпускаются по рецепту, который можно получить у эндокринолога.
Существует два типа таблеток:
- стандартные, например, Сиофор (Metformax);
- с медленным высвобождением, например, Глюкофаж (Metformax SR).
Стандартные препараты действуют быстро. В зависимости от дозы может потребоваться принимать их несколько раз в день. Обычно терапия начинается с наименьшей дозировки, которая модифицируется эндокринологом на основании полученных измерений уровня сахара через 10-15 дней. Максимальные суточные дозы составляют 2000-3000 мг в 2-4 приема.
Таблетки медленного высвобождения растворяются медленно, поэтому их не нужно принимать часто. Обычно одной порции препарата достаточно для приема во время ужина.
Для препаратов стандартного выпуска рекомендуется медленное увеличение дозы. Это уменьшает вероятность побочных эффектов. Но увлекаться большой дозировкой бессмысленно: исследования показывают, что увеличение дозы от 2000 до 3000 мг улучшает контроль диабета незначительно.
Метформин – эффекты и клиническая эффективность
В последние годы диабет 2 типа все чаще признается одним из основных факторов риска развития сердечно-сосудистых заболеваний. Наиболее распространенное осложнение этого заболевания среди европейцев – атеросклероз, встречающийся в 2-5 раз чаще у людей с диабетом, чем у здоровых людей.
Эти наблюдения показывают, что лечение диабета требует мер, которые не только снижают уровень глюкозы в крови, но и оказывают гипогликемическое и улучшающее воздействие на:
- дислипидемию;
- гипертонию;
- ожирение;
- гиперинсулинемию;
- резистентность к инсулину.
Прием метформина в правильных дозах может принести наибольшую пользу в этом направлении. Было показано, что он снижает уровень глюкозы, триглицеридов и помогает снизить вес.
Согласно исследованиям, основным метаболическим расстройством при ожирении и диабете типа 2 является резистентность к инсулину. Таким образом, хорошо известное влияние метформина на снижение резистентности к инсулину делает этот препарат отличным средством для предотвращения прогрессирования нарушения толерантности к глюкозе и снижения смертности от сердечно-сосудистых патологий.
Метформин – побочные эффекты и противопоказания
Побочные эффекты приема метформина чаще всего возникают только в начале терапии и в большинстве случаев через некоторое время проходят самостоятельно, после того как организм привыкнет к лекарству.
В начале лечения пациенты часто жалуются на:
- нарушение вкуса;
- расстройство аппетита;
- тошноту;
- рвоту;
- понос;
- боль в животе.
Использование препарата в нормах, выписанных эндокринологом, не несет риска гипогликемии. Но нужно быть осторожнее при одновременном приеме нескольких противодиабетических средств. Комбинация метформина с другими сахароснижающими препаратами или инсулином может привести к падению уровня глюкозы до опасного для жизни уровня.
Также опасен одновременный прием метформина с алкоголем – может развиться лактоацидоз.
Противопоказания к применению этого препарата: почечная недостаточность, печеночная недостаточность, беременность и кормление грудью.
ИНСТРУКЦИЯ
по медицинскому применению лекарственного препарата
Торговое наименование препарата
Международное непатентованное наименование
Лекарственная форма
таблетки покрытые оболочкой
Состав
Состав на 1 таблетку:
Действующее вещество: метформина гидрохлорид - 850,0 мг;
Вспомогательные вещества: гипромеллоза - 30,0 мг, повидон - 45,0 мг, магния стеарат - 5,0 мг.
Оболочка: гипромеллоза - 10,0 мг, макрогол 6000 - 2,0 мг, титана диоксид, Е 171 - 8,0 мг.
Описание
Фармакотерапевтическая группа
Гипогликемическое средство для перорального применения группы бигуанидов
Код АТХ
Фармакодинамика:
Метформин относится к группе бигуанидов. Обладает гипогликемическим действием. Обеспечивает снижение как базальной так и постпрандиальной концентрации глюкозы в плазме крови. Не стимулирует секрецию инсулина и поэтому не приводит к гипогликемии.
Действие метформина основывается на следующих механизмах:
- снижение выработки глюкозы в печени вследствие угнетения глюконеогенеза и гликогенолиза;
- повышение чувствительности мышц к инсулину и следовательно улучшение поглощения и утилизации глюкозы на периферии;
- угнетение всасывания глюкозы в кишечнике.
Метформин посредством действия на гликогенсинтазу стимулирует внутриклеточный синтез гликогена. Повышает транспортную емкость всех известных до настоящего времени мембранных транспортных протеинов глюкозы.
Обладает независимо от его влияния на концентрацию глюкозы в плазме крови благоприятным действием на липидный обмен приводит к снижению концентрации общего холестерина холестерина липопротеидов низкой плотности и триглицеридов.
На фоне применения метформина у пациентов с сахарным диабетом масса тела либо остается стабильной либо умеренно снижается.
Фармакокинетика:
После приема препарата внутрь метформин абсорбируется практически полностью из желудочно-кишечного тракта максимальная концентрация (Сmах) в плазме крови достигается через 25 ч и при максимальной дозе не превышает 4 мкг/мл. Прием пищи уменьшает степень всасывания (Сmах снижается на 40 % площадь под кривой "концентрация-время" (AUC) на 25 %) и слегка замедляет всасывание метформина из желудочно-кишечного тракта (время достижения Сmах снижается на 35 минут). При применении в рекомендуемых дозах равновесная концентрация в плазме крови достигается в течение 24-48 ч и как правило не превышает 1 мкг/мл. Абсолютная биодоступность у здоровых добровольцев составляет приблизительно 50 - 60 %.
Практически не связывается с белками плазмы крови. Проникает в эритроциты. Сmах в крови ниже Сmах в плазме крови и достигается примерно за то же время. Вероятно эритроциты представляют собой вторичный компартмент распределения. Средний объем распределения (Vd) составляет 63-276 л.
Метаболизм и выведение
Выводится почками в неизмененном виде. Метаболитов в организме человека не обнаружено. Почечный клиренс составляет > 400 мл/мин. Период полувыведения (T1/2)составляет около 65 ч. При снижении функции почек клиренс метформина снижается пропорционально клиренсу креатинина соответственно период полувыведения удлиняется и концентрация метформина в плазме крови повышается.
При однократном применении метформина у детей в дозе 500 мг фармакокинетические параметры были сходны с таковыми у взрослых.
Показания:
Сахарный диабет 2 типа особенно у пациентов с избыточной массой тела для контроля концентрации глюкозы в плазме крови.
- у взрослых в качестве монотерапии или в составе комбинированной терапии с другими пероральными гипогликемическими средствами и/или инсулином.
- у детей старше 10 лет в качестве монотерапии или в комбинации с инсулином.
Лечение сахарного диабета 2 типа должно сопровождаться коррекцией диеты и повышением физической активности (при отсутствии противопоказаний).
Противопоказания:
- гиперчувствительность к метформину или вспомогательным веществам препарата;
- диабетический кетоацидоз диабетическая прекома кома;
- нарушение функции почек (клиренс креатинина Нарушения со стороны нервной системы:
Часто: нарушение вкуса.
Нарушения со стороны желудочно-кишечного тракта:
Очень часто: тошнота рвота диарея боль в животе потеря аппетита.
Эти нежелательные явления часто возникают в начале терапии и в большинстве случаев проходят самопроизвольно. Для предотвращения симптомов дозу препарата рекомендуется распределять на 2-3 приема во время или после еды. Постепенное увеличение дозы улучшает переносимость препарата со стороны желудочно-кишечного тракта.
Нарушения со стороны кожи и подкожных тканей:
Очень редко: кожные реакции например эритема зуд сыпь.
Нарушения со стороны обмена веществ и питания:
Очень редко: лактоацидоз (требует прекращения лечения). Симптомы лактоацидоза - см. раздел "Передозировка".
При длительном применении наблюдается уменьшение всасывания витамина В12 и снижение его концентрации в плазме крови. Это следует учесть при наличии у больного мегалобластной анемии.
Нарушения со стороны печени и желчевыводящих путей:
Очень редко: обратимые нарушения функции печени выражающиеся в повышении активности печеночных трансаминаз или гепатит проходящие после прекращения приема метформина.
Согласно данным полученным в ходе пострегистрационного применения и результатам контролируемых клинических исследований при применении метформина в течение 1 года у детей в возрасте 10-16 лет частота возникновения и выраженность побочных эффектов была сопоставима с таковыми для взрослых.
Передозировка:
При применении метформина в дозах до 85 г гипогликемии не наблюдалось.
При значительной передозировке возможно развитие лактоацидоза симптомами которого являются выраженная слабость респираторные нарушения сонливость тошнота рвота диарея боль в животе гипотермия снижение артериального давления рефлекторная брадиаритмия. Могут отмечаться мышечные судороги спутанность и потеря сознания. При подозрении на развитие лактоацидоза рекомендуется немедленная отмена препарата и экстренная госпитализация.
Наиболее эффективный метод удаления лактата и метформина из организма - гемодиализ.
Взаимодействие:
Одновременное применение противопоказано
Йодсодержащие рентгеноконтрастные средства
Внутрисосудистое введение йодсодержащих рентгеноконтрастных средств у пациентов с сахарным диабетом может осложниться почечной недостаточностью вследствие чего метформин кумулирует и повышается риск развития лактоацидоза. Применение препарата Сиофор® 850 следует отменить в течение 48 ч до и не возобновлять ранее чем через 48 ч после рентгенологического исследования с использованием йодсодержащих рентгеноконтрастных средств при условии нормальной концентрации сывороточного креатинина.
Одновременное применение не рекомендуется
Алкоголь и этанолсодержащие препараты
Риск развития лактоацидоза увеличивается при острой алкогольной интоксикации или одновременном применении с этанолсодержащими препаратами особенно на фоне голодания или нарушения питания а также печеночной недостаточности. Во время приема метформина следует избегать приема алкоголя и лекарственных средств содержащих этанол.
Одновременное применение требует осторожности
Одновременное применение метформина с даназолом может привести к развитию гипергликемического эффекта. При необходимости лечения даназолом и после прекращения его применения требуется коррекция дозы метформина под контролем концентрации глюкозы в плазме крови.
Хлорпромазин: при применении в больших дозах (100 мг в день) повышает концентрацию глюкозы в плазме крови снижая высвобождение инсулина. При лечении нейролептиками и после прекращения применения последних требуется коррекция дозы метформина под контролем концентрации глюкозы в плазме крови.
При одновременном применении с пероральными контрацептивными средствами эпинефрином глюкагоном гормонами щитовидной железы производными фенотиазина никотиновой кислотой возможно повышение концентрации глюкозы в плазме крови. Нифедипин повышает абсорбцию максимальную концентрацию метформина в плазме крови пролонгирует его выведение.
Катионные препараты (амилорид морфин прокаинамид хинидин хинин ранитидин триамтерен ванкомицин) секретирующиеся в канальцах конкурируют за канальцевые транспортные системы и при длительной терапии могут увеличить максимальную концентрацию метформина в плазме крови. Метформин уменьшает максимальную концентрацию и период полувыведения фуросемида; может ослабить эффект антикоагулянтов непрямого действия.
Глюкокортикоиды (системное и местное применение) бета2-адреномиметики (в виде инъекций) обладают гипергликемической активностью. Следует более тщательно контролировать концентрацию глюкозы в плазме крови особенно в начале лечения. При необходимости дозу метформина следует скорректировать на период одновременного применения а также после отмены этих препаратов.
При одновременном применении с диуретиками особенно "петлевыми" возможно повышение риска развития лактоацидоза ввиду потенциальной способности диуретиков снижать функцию почек.
Ингибиторы АПФ и другие гипотензивные лекарственные средства могут снижать концентрацию глюкозы в плазме крови. При необходимости доза метформина может быть скорректирована.
Субстраты транспортера органических катионов 2 (ОСТ2)
При одновременном применении ранолазина 500 мг и 1000 мг 2 раза в сутки и метформина 1000 мг 2 раза в сутки концентрация метформина в плазме крови у пациентов с сахарным диабетом 2 типа повышается в 14 и в 18 раз соответственно.
При одновременном применении 400 мг циметидина два раза в сутки у 7 здоровых добровольцев AUC и Сmaх метформина увеличились на 50 % и на 81 % соответственно. При одновременном применении метформина с производными сульфонилмочевины инсулином акарбозой салицилатами возможно усиление гипогликемического действия.
Особые указания:
Лактоацидоз - серьезное патологическое состояние встречающееся крайне редко связанное с накоплением в крови лактата причиной которого может стать кумуляция метформина (симптомы лактоацидоза - см. раздел "Передозировка"). Диагностическими лабораторными показателями лактоацидоза являются снижение pH крови менее 725 содержание лактата в плазме крови свыше 5 ммоль/л повышенные анионный промежуток и отношение лактат/пируват. Описанные случаи развития лактоацидоза у пациентов получавших метформин наблюдались преимущественно у пациентов с сахарным диабетом с выраженной почечной недостаточностью. Профилактика лактоацидоза предполагает определение всех сопутствующих факторов риска таких как декомпенсированный сахарный диабет кетоз длительное голодание чрезмерное употребление алкоголя печеночная недостаточность и любое состояние связанное с гипоксией. При подозрении на развитие лактоацидоза рекомендуется немедленная отмена препарата и экстренная госпитализация.
Поскольку метформин выводится почками при применении препарата Сиофор® 850 должен регулярно осуществляться контроль концентрации сывороточного креатинина:
- не менее одного раза в год у пациентов с нормальной функцией почек;
- не менее 2-4 раз в год у пациентов с концентрацией сывороточного креатинина близкой к верхней границе нормы а также у пожилых пациентов.
Особую осторожность следует соблюдать в тех случаях когда возникает риск нарушения функции почек например в начале терапии гипотензивными препаратами диуретиками или нестероидными противовоспалительными препаратами (НПВП).
Лечение препаратом Сиофор® 850 необходимо временно заменить терапией другими гипогликемическими средствами (например инсулином) в течение 48 ч до и 48 ч после рентгенологического исследования с внутривенным введением йодсодержащих рентгеноконтрастных средств.
Применение препарата Сиофор® 850 необходимо прекратить в течение 48 ч до плановой хирургической операции под общим наркозом со спинальной или эпидуральной анестезией. Продолжить терапию следует после возобновления перорального питания или не ранее чем через 48 ч после хирургического вмешательства при условии подтверждения нормальной почечной функции.
Препарат Сиофор® 850 не заменяет диету и ежедневные физические упражнения - эти виды терапии необходимо сочетать в соответствии с рекомендациями врача. Во время лечения препаратом Сиофор 850 всем пациентам следует придерживаться диетического питания с равномерным потреблением углеводов в течение дня. Пациенты с избыточной массой тела должны соблюдать низкокалорийную диету.
Стандартные для пациентов с сахарным диабетом лабораторные исследования необходимо проводить регулярно.
Перед применением препарата Сиофор® 850 у детей от 10 до 18 лет следует подтвердить диагноз сахарного диабета 2 типа.
В ходе контролируемых клинических исследований продолжительностью 1 год влияния метформина на рост и развитие а также половое созревание детей не наблюдалось данные по этим показателям при более длительном применении отсутствуют. В связи с этим рекомендуется тщательный контроль соответствующих параметров у детей получающих метформин особенно в препубертатный период (10-12 лет).
Монотерапия препаратом Сиофор® 850 не приводит к гипогликемии однако рекомендуется соблюдать осторожность при совместном применении препарата с инсулином или производными сульфонилмочевины.
Метформин не влиял на фертильность самцов или самок крыс при применении в дозах (600 мг/кг/сут) втрое превышающих максимальную рекомендованную суточную дозу для человека.
Влияние на способность управлять трансп. ср. и мех.:
Применение препарата Сиофор® 850 не вызывает гипогликемию поэтому не влияет на способность к управлению транспортными средствами и обслуживанию механизмов.
При одновременном применении препарата Сиофор® 850 с другими гипогликемическими лекарственными средствами (производные сульфонилмочевины инсулин репаглинид) возможно развитие гипогликемических состояний поэтому необходимо соблюдать осторожность при управлении транспортными средствами и другими потенциально опасными видами деятельности требующих концентрации внимания и быстроты психомоторных реакций.
Форма выпуска/дозировка:
Упаковка:
По 15 таблеток в контурную ячейковую упаковку (блистер) [ПВХ-пленка/фольга алюминиевая].
По 2 4 или 8 блистеров вместе с инструкцией по применению помещают в картонную пачку.
Условия хранения:
При температуре не выше 25 °С.
Лекарственное средство хранить в недоступном для детей месте!
Срок годности:
Не применять по истечении срока годности указанного на упаковке.
Условия отпуска
Производитель
Берлин-Хеми АГ, Glienicker Weg 125, 12489, Berlin, Germany, Германия
Каждый этап жизни волоса контролируют гормоны. Неудивительно, что после заболеваний и потрясений, провоцирующий гормональный сбой, состояние локонов резко ухудшается. В частности, выпадение волос излечить очень сложно, если не учитывать гормональный фактор. Мы решили рассказать о нем подробнее.
Что такое гормоны?
Гормоны — это специфические сигнальные молекулы, своего рода нашего тела. Они разносятся с током крови и несут в себе биологическую информацию, которая активирует либо тормозит реакции в клетках и тканях. Благодаря гормонам регулируются все процессы в организме: происходит его рост, половое созревание, возрастные изменения. этих биоактивных веществ мы испытываем чувство голода и насыщения, сексуальное влечение, гнев или радость. От работы гормональной системы зависит и качество нашего иммунитета.
Гормоны бывают:
- стероидные (липидные) — растворяются в жире (именно поэтому их называют липидными, жировыми); они не могут самостоятельно перемешаться, пользуются помощью ;
- белковые — растворяются в воде, двигаются к самостоятельно.
Выработку гормонов регулирует центральная нервная система, а непосредственно в их производстве задействована эндокринная. Нервный импульс от тканей и органов поступает в мозг, там обрабатывается и передается в гипоталамус. Эта структура вырабатывает статины (замедлители) или тропины (стимуляторы). Данные вещества воздействуют на гипофиз, и уже он координирует работу надпочечников, щитовидной, паращитовидной и половых желез, которые и вырабатывают гормоны.
Важно! Хотя нет специальных гормонов, отвечающих за выпадение волос, именно гормональный баланс или дисбаланс определяет густоту и красоту нашей шевелюры. Интересно, что липидные гормоны умеют контролировать даже процесс считывания генетической информации: они могут запускать или блокировать работу отдельных генов.
Какие гормоны влияют на выпадение волос?
Равновесие — это ключ к здоровью прядей, если мы говорим о гормонах. Однако естественные колебания гормонального фона сопровождают нас всю жизнь, и соответственно этому меняется наша шевелюра. Вот мы понервничали, и через время видим клочья волос на расческе. А за время беременности локоны отрастают, становятся гуще, укрепляются.
Гормональный баланс может меняться целого ряда причин:
- возраста;
- стресса;
- эндокринных патологий и нарушений;
- приема гормональных лекарственных средств и др.;
- приема противозачаточных таблеток;
- перестройки организма (беременность, климакс).
При этом среди всех причин потери волос влияние гормонов остается доминирующим (в группе повышенного риска — люди с наследственной предрасположенностью). Попытаемся разобраться, какие гормоны влияют на выпадение волос и каким образом.
Влияние андрогенов на рост волос
Андрогены — это мужские половые стероидные гормоны. Хотя их называют мужскими, они есть в организме как мужчин, так и женщин, однако в разных пропорциях и с разной «целью».
Процесс гормональной настройки начинается еще в материнской утробе: в зависимости от генов, у эмбриона становятся активными разные типы рецепторов. У девочек они будут реагировать на эстроген, у мальчиков — на тестостерон (подвид андрогенов) матери. Эта генетическая восприимчивость к разным гормонам полностью определит дальнейшее развитие человека.
От количества маскулинных (мужских) биоактивных веществ в крови и восприимчивости к ним зависит размер половых органов, высота голоса (чем больше андрогенов, тем он ниже), оволосение лица и тела. Если уровень таких гормонов высок, омужествление тела (гирсутизм) может начаться у женщин любого возраста.
В организме и мужчин, и женщин андрогены:
- стимулируют обмен веществ;
- запускают обновление клеток;
- вызывают рост мышечной ткани;
- укрепляют кости кальцием и специальными структурными компонентами.
Как андрогены влияют на рост волос? Андрогены — главные дирижеры роста волос человека. Именно они запускают процесс превращения тонких пушковых волос в зрелые, взрослые. Однако они же могут вызывать и деградацию волосков на некоторых участках головы.
Интересно, что разные волосяные фолликулы реагируют на андрогены. Так, эти биоактивные вещества:
- могут приводить к ослаблению роста волос на темени, макушке и висках;
- активизируют рост усов, бороды, бакенбардов и волос на теле;
- не оказывают практически никакого воздействия на затылочные волосяные фолликулы.
Эта особенность учитывается при трансплантации волосков — для устранения андрогенной алопеции в зоны облысения пересаживают фолликулы, «нечувствительные» к мужским половым гормонам.
Когда возникает выпадение волос? Алопеция у женщин и мужчин андрогенов бывает в нескольких случаях:
- генетической предрасположенности;
- по причине заболеваний, влияющих на увеличение производства мужских гормонов.
Наследственность может сделать ваши рецепторы чрезмерно чувствительными к ДГТ, активной форме андрогенов — дигидротестостерону. Именно эта форма, накапливаясь в фолликулах, приводит к тому, что волоски истончаются все больше и больше, пока не прекращают свой рост полностью. Отмершие луковицы со временем замещаются соединительной тканью, и в этих случаях восстановить рост волос практически невозможно.
От генетических особенностей зависит и количество производимых андрогенов — так, нарушенный синтез кортизола, гормона надпочечников, может вызывать избыток производства андрогенов, и следовательно — переизбыток ДГТ.
Превышение норм андрогенов возникает в результате множества болезней:
- поликистоза и новообразований в яичниках;
- гиперплазии либо очагового разрастания клеток надпочечников;
- синдрома гиперкортицизма;
- новообразований молочной железы, гипофиза
Важно! Ученые выяснили, что и у мужчин, и у женщин так называемый сосочковый слой кожи и сами волосяные фолликулы вырабатывают тестостерон и трансформируют его в ДГТ. Так что даже если в сыворотке крови определен недостаток андрогенов, выпадение волос все равно может вызываться этими гормонами, но только местно.
Эстроген и состояние волос
Эстрогены — это гормоны, которые преимущественно вырабатываются придатками яичников, поэтому их называют женскими гормонами. Также их производят надпочечники. Именно благодаря настроенности рецепторов на эстроген, женское тело отличается от мужского.
В организме эстрогены:
- влияют на рост волосяного фолликула и цикличность его работы;
- делают кожу гладкой, увлажненной, упругой;
- дают ощущение бодрости, энергичности;
- стабилизируют настроение;
- повышают либидо.
Как женские половые гормоны влияют на рост волос? Повышение эстрогена в совокупности с прогестероном удерживает волосы в фазе активного и длительного роста (стадия анагена). Именно этим объясняется то, что во время беременности, когда количество эстрогенов в крови повышается, локоны женщин становятся максимально густыми и пышными. Во время климакса шевелюра наоборот редеет и слабеет, уровень эстрогенов снижается.
Почему возникает выпадение волос? На сегодняшний день ученые предполагают, что процесс алопеции в связи с женскими половыми гормонами может запускать:
- генетика;
- менопауза;
- отдельные заболевания яичников, почек, эндокринной системы;
- отмена приема ОК (оральных контрацептивов);
- воздействие эндокринных разрушителей (источники: косметика с фталатами, пластик, нефильтрованная вода и проч).
Причем негативные последствия, включающие облысение, наступают не просто уменьшения или увеличения количества женского гормона, а нарушения процентного соотношения эстрогенов к андрогенам, а также прогестерону. Уровень эстрогена и прогестерона должен быть одинаков, иначе локоны станут слабыми, хрупкими, существенно поредеют.
Важно! Часто в послеродовый период женщины переживают: «Что делать? Катастрофически выпадают волосы!» На самом деле волосяные фолликулы просто возвращаются к своему привычному ритму работы, без подстегивания избытком эстрогенов. через три месяца это «стихийное» поредение шевелюры прекратится.
Йодсодержащие пептиды и их влияние на локоны
Гормоны щитовидной железы иначе называют тиреотропными, а также йодсодержащими пептидами. Они воздействуют на:
- развитие и работу ЦНС;
- рост тканей организма;
- функционирование системы;
- метаболизм;
- моторику кишечника;
- менструальный цикл и репродуктивную сферу в целом;
- состояние органов слуха и зрения.
Какое влияние оказывают эти гормоны на локоны? Для наших прядей значение биоактивных веществ, которые производит щитовидная железа, огромно — с их помощью волоски формируются в фолликулах и растут.
- Указанные гормоны регулируют кислородный баланс в клетках;
- управляют синтезом белка;
- отвечают за здоровое деление клеток.
Если показатели гормонов щитовидной железы в норме, это обеспечивает волосяным фолликулам достаточную продолжительность периода интенсивного роста.
В каких случаях начинается выпадение волос? При заболеваниях щитовидной железы йодсодержащих гормонов вырабатывается много либо недостаточно. Любое из отклонений может повлечь за собой алопецию.
- Гипертиреоз — характеризуется избытком циркулирующих в крови тиреотропинов. В 25–50% случаев вызывает поредение прядей по всей голове. Локоны становятся слабыми, очень мягкими, прямыми — настолько, что не поддаются никакой завивке, даже перманентной. Отличительной чертой гипертиреоза является также потеря волос подмышками.
- Гипотиреоз — состояние, возникающее от недостатка гормонов щитовидной железы. У женщин заболевание возникает в 10 раз чаще, чем у мужчин, особенно после менопаузы. болезни волосы становятся тонкими, тусклыми, слабыми, интенсивно выпадают. Характерная особенность — редеет не только шевелюра, но и брови. Стадия анагена волосяных фолликулов существенно сокращается, увеличивается количество луковиц в стадии телогена (отмирания). Кроме того, при гипотериозе резко возрастают показатели андрогенов в сыворотке крови, что усугубляет течение алопеции.
- Гипопаратиреоз — развивается по причине иссечения паращитовидных желез в случае оперативного вмешательства на щитовидной железе. Волосы истончаются вплоть до полного облысения.
- Причиной поредения волос и алопеции бывают медпрепараты для терапии болезней щитовидки: йод, левотироксин, карбимазол, тиамазол, литий, амиодарон, метилтиоурацил, пропилтиоурацил.
Важно! Начинать восстановление прядей нужно с поиска причины их поредения. Импульсивные покупки шампуней, бальзамов, биодобавок, а тем более стремление пропить тот или иной гормональный препарат «против выпадения волос» могут существенно усугубить проблемы с шевелюрой и здоровьем в целом.
Лечение выпадения волос и его предупреждение
Чтобы вернуть волосам здоровье, нужно восстановить баланс гормонов в организме. Это можно сделать путем приема соответствующих гормональных препаратов. Либо проблема решается после выздоровления, если гормональное нарушение было вызвано заболеванием.
Для начала необходимо пройти комплексное обследование:
- сдать анализы крови — общий, биохимический, на содержание глюкозы, железа и на гормоны;
- сделать УЗИ репродуктивных и эндокринных органов;
- сделать рентген мозга;
- пройти консультацию у эндокринолога;
- посетить других специалистов (в зависимости от анамнеза).
Какие конкретно гормоны нужно сдать при выпадении волос?
- репродуктивной системы (женщинам — на 5–9 день менструального цикла) — эстрогены, андрогены;
- прогестерон (женщинам — на 21 день цикла);
- кортизол;
- адреналин;
- тиреотропные гормоны (ТТГ, Т3, Т4, тиреоглобулин).
После всестороннего обследования доктор определит, какой гормон отвечает за выпадение волос в вашей ситуации. Но обычно гормональный дисбаланс, осложненный облысением — комплексная проблема, которая требует такого же решения. Больному назначают:
- процедуры, направленные на оздоровление всего организма;
- лечебное питание;
- медикаменты и процедуры для лечения определенных органов или систем;
- индивидуально подобранные гормональные препараты;
- местно действующие средства (чаще всего, шампуни и бальзамы с миноксидилом);
- поливитамины;
- физиотерапевтические процедуры (дарсанваль, крио- и лазеротерапию и др.).
Врач также посоветует, как изменить режим, чтобы снизить действие вредных внутренних и внешних факторов на волосы.
Лечение гормональной алопеции — процесс длительный. Первые результаты будут заметны лишь спустя три месяца, в случае скрупулезного соблюдения всех рекомендаций специалиста.
И все же иногда этого оказывается мало. Современная медицина предлагает оперативный метод лечения алопеции — трансплантацию волос. Сегодня распространен щадящий метод HFE, который считается малоинвазивным. Во время процедуры почти не используется анестезия, а после пациент может отправляться домой, а не оставаться в условиях стационара.
Важно! Гормональные препараты, устраняющие проблему, необходимо пить долгое время, иногда всю жизнь. Если вам назначены медикаменты, не забывайте раз в три месяца посещать врача для коррекции дозировки, иначе все симптомы дисбаланса гормонов, включая алопецию, могут вернуться.
Если есть хоть малейший риск гормонального выпадения волос, необходимо особое внимание уделять профилактике. Ежегодно проходите полный медицинский осмотр, следя, чтобы гормоны были в норме. А ежедневный качественный уход за волосами, сбалансированное питание, налаженный режим труда и отдыха помогут вашим локонам всегда оставаться густыми и здоровыми.
Миноксидил – популярный препарат, который привыкли назначать при выпадении волос. Однако, это не единственный эффективный и не самый безопасный способ борьбы с алопецией. Чем опасен миноксидил и чем его можно заменить? Расскажем в этой статье.
Что такое миноксидил?
Миноксидил – это сосудорасширяющий гипотензивный препарат, побочным действием которого является стимуляция роста волос. Причем изначально этот препарат был создан для лечения язвы желудка, для чего оказался бесполезным, но проявились его сосудорасширяющие свойства. Как следствие его начали использовать для понижения давления, в ходе чего обнаружился следующий побочный эффект – рост волос. При этом механизм, посредством которого миноксидил влияет на рост волос, до конца не известен и не изучен. Предположительно, эффект достигается за счет расширения кровеносных сосудов, что способствует увеличению доступа крови, кислорода и питательных веществ в волосяные луковицы. Получив питание и кислород, фолликулы начинают работать активнее, производя более крепкий и толстый волос.
Почему миноксидил так популярен?

Миноксидил стал уже традиционным средством, которое назначают во всем мире для лечения алопеции, особенно – андрогенетической (АГА). Назначают, несмотря на его многочисленные противопоказания и побочные эффекты, которые миноксидил имеет как любой лекарственный препарат. Дело в том, что долгое время не было альтернативы – миноксидил был практически единственным препаратом, который давал эффект. К нему привыкли и врачи, и пациенты. На сегодняшний день появились не менее эффективные и при этом безвредные средства, о чем говорят все продвинутые трихологи. Но сила привычки в совокупности с «миноксидиловым» бизнесом порой не дает обычным потребителям возможности узнать правду.
При этом сам факт того, что миноксидил назначают «всем подряд», вне зависимости от пола и причин выпадения, уже должно настораживать. Ведь не существует универсальной терапии, например, сердечно-сосудистых или бактериальных заболеваний – лечение всегда подбирается индивидуально и, как правило, является комплексным.
Противопоказания для использования миноксидила:
- Хронические заболевания кровеносной системы;
- Кожные заболевания в острой форме;
- Инфекционные заболевания;
- Опухоли (препарат не вызывает рост новообразований, но повышает риск их метастазирования);
- Открытые раны (порезы, ссадины), язвы, ожоги на коже головы;
- Беременность и период лактации;
- Возраст до 18 и старше 65 лет.
Чем опасен миноксидил?
Во-первых, побочными действиями:
- Головные боли;
- Головокружения;
- Учащенное сердцебиение, боли в сердце;
- Нежелательный рост волос на лице;
- Раздражение кожи головы, жжение, сухость, стянутость;
- При сухом типе кожи головы – возможны себорея и перхоть;
- Отеки рук и ног;
- Редко - аллергические реакции.
Также владельцем домашних животных важно знать, что миноксидил крайне токсичен для кошек и при контакте вызывает отравление вплоть до летального исхода.
Во-вторых, это привыкание и ярко выраженный синдром отмены.
Главная опасность миноксидила кроется в том, что со временем – через 2-3 года систематического применения – капилляры, которые исправно расширялись под действием миноксидила все эти годы, перестают расширяться и становятся больше не чувствительны к действию компонентов миноксидила. Луковицы, привыкшие за это время получать обильное питание, перестают его получать, и начинается интенсивное выпадение. По этой причине появляются все более высокие дозировки миноксидила: в 80-е это было 2%, в 90-е появился миноксидил 5%, сейчас доходит до 15%. Чем больше дозировка – тем больше побочных действий. К тому же в препараты с миноксидилом начинают добавлять различные сильнодействующие вещества, в том числе гормоны, чтобы как-то сохранить его эффект для тех, кто пользуется миноксидилом давно. Вы становитесь «заложником» миноксидила – вам приходится использовать его постоянно и постоянно увеличивать дозировку.
Миноксидил – это препарат, которым нужно пользоваться очень долго, либо, в случае ярко выраженной АГА у мужчин, – пожизненно. И если миноксидил вызывает у вас побочные эффекты, то это становится либо опасным, либо вовсе невозможным.
Как «слезть» с миноксидила?
Если вы используете миноксидил недавно и не каждый день (2-3 раза в неделю или хотя бы через день), то вам следует постепенно переходить на безопасную частоту применения – 1 раз в 7-10 дней.
Если же вы систематически применяете миноксидил уже более года, то процесс отвыкания займет не менее 2-3 месяцев. Трихологи рекомендуют следующую схему:
В течение первых 2-3 недель переходим с ежедневного применения миноксидиа на использование через день и наблюдаем. Если выпадение волос не увеличивается – то переходим к следующему этапу. Если же выпадение усиливается, добавляем другие средства: витаминные комплексы (внутрь), лосьоны и сыворотки без миноксидила (наружно);
Следующие 2-3 недели используем миноксидил с частотой 1-2 раза в неделю.
За следующие 2-3 недели наша задача перейти к графику применения 1 раз в 7-10 дней.
Сразу отметим, что очень часто «слезть» с миноксидила самостоятельно не получается, и лучше воспользоваться помощью специалиста.
Как распознать миноксидил?
Сегодня средства с миноксидилом выпускают различные производители под разными названиями. Поэтому будьте внимательны и читайте состав на этикетке – ищите действующее вещество «minoxidil». Такие средства разрешено продавать только в аптеках – вы не встретите их в косметических магазинах. Однако существует популярный аналог миноксидила – аминексил (облегченная версия миноксидила). Его разрешено включать в состав косметических средств и поэтому можно купить где угодно. Но по своим недостаткам он схож с миноксидилом, поэтому нужно внимательно изучать состав при покупке даже косметических средств против выпадения. Аминексил обозначается как «aminexil».
Эффективная и безопасная альтернатива
Миноксидил, помимо своих недостатков, помогает не всем. Поэтому, даже если вы решились на использование миноксидила, не стоит выбирать его как монотерапию. Лечение выпадения волос всегда должно быть комплексным, и если в нем и будет присутствовать миноксидил, используйте его не чаще 1 раза в 7-10 дней.
Терапия должна быть разнонаправленной. Она может включать в себя и прием витаминных комплексов, и косметологические процедуры, и использование наружных средств на основе витаминов, аминокислот, растительных экстрактов, пептидов.
Какой набор средств поможет именно вам? На этот вопрос ответит только грамотный врач-трихолог. Он же, при необходимости, может назначить вам консультации с другими специалистами, если, например, выпадение связано с нарушением кровообращения из-за шейного остеохондроза либо гормональным дисбалансом.
Также следует понимать, что миноксидил может повлиять только на одну причину выпадения волос – ухудшение местного кровообращения. При этом потеря объема может быть связана и с другими факторами:
- дефицитом питательных веществ;
- действием гормона дигидротестостерона (ДГТ), вызывающего дистрофию волосяных луковиц при АГА;
- низкими темпами либо отсутствием роста новых волос.
Современные средства борьбы с выпадением влияют сразу на все эти причины, помогая и улучшить местный кровоток, и напитать корни необходимыми веществами, и блокировать ДГТ, а также стимулировать рост новых волос с помощью безопасных факторов роста. К таким средствам относятся сыворотки на основе пептидов, витаминов и растительных экстрактов. При этом они не имеют побочных действий, противопоказаний, синдрома отмены и не вызывают привыкания. Сыворотки с пептидами являются достойной и безопасной альтернативой средствам с миноксидилом и его аналогами, поэтому сегодня уже нет необходимости мириться с недостатками миноксидила.
Читайте также:

